0 126924 126932 126938 126942 126948 126950 126954 126960 126962 126968 126974 126978 126980 126984 126990 126992 126998 127002 127004 127008 127010 127014 127016 127018 127019 127020 127022 127023 127024 127026 127028 127032 127034 127038 127040 127044 127050 127052 127058 127062 127064 127068 127074 127080 127082 127088 127092 127094 127100 127104 127110 127118 211419
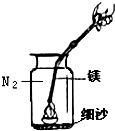 林林做镁带在空气中燃烧实验时,发现生成的白色固体的质量小于参加反应的金属镁和氧气的质量和.他在一本参考书上发现,镁居然能在氮气中燃烧!于是他做起了这个实验:将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁(Mg3N2)的粉末.
林林做镁带在空气中燃烧实验时,发现生成的白色固体的质量小于参加反应的金属镁和氧气的质量和.他在一本参考书上发现,镁居然能在氮气中燃烧!于是他做起了这个实验:将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁(Mg3N2)的粉末.

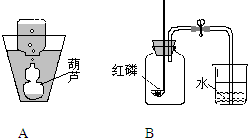 空腔果实内由于不发生光合作用,其中的气体可能与空气产生差异,某同学选择一个熟透的葫芦,按下列方案进行研究:
空腔果实内由于不发生光合作用,其中的气体可能与空气产生差异,某同学选择一个熟透的葫芦,按下列方案进行研究: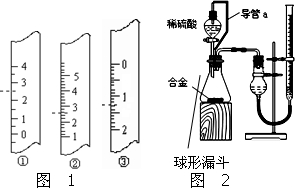 铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.