0 126580 126588 126594 126598 126604 126606 126610 126616 126618 126624 126630 126634 126636 126640 126646 126648 126654 126658 126660 126664 126666 126670 126672 126674 126675 126676 126678 126679 126680 126682 126684 126688 126690 126694 126696 126700 126706 126708 126714 126718 126720 126724 126730 126736 126738 126744 126748 126750 126756 126760 126766 126774 211419
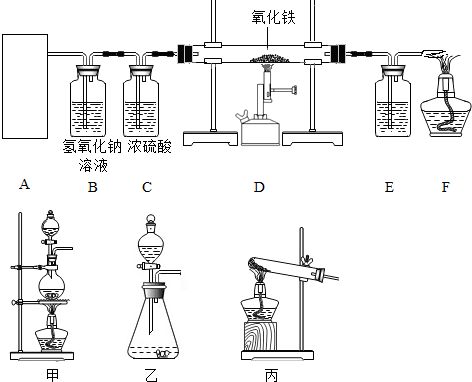
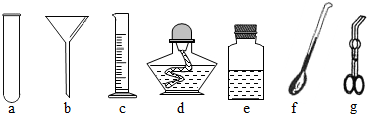

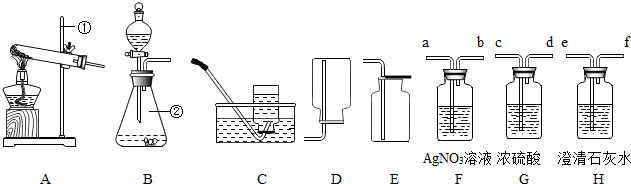
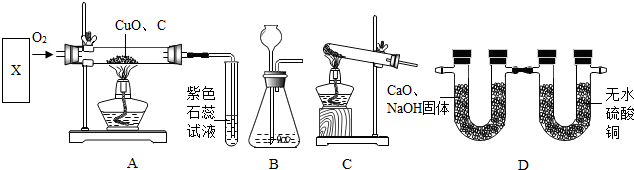

 某初级中学学生为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图1所示)可能是什么物质,大胆猜想并设计实验进行验证.
某初级中学学生为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图1所示)可能是什么物质,大胆猜想并设计实验进行验证.