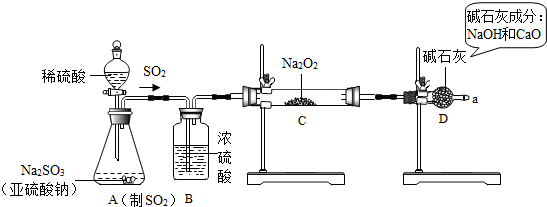
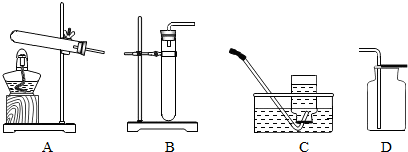
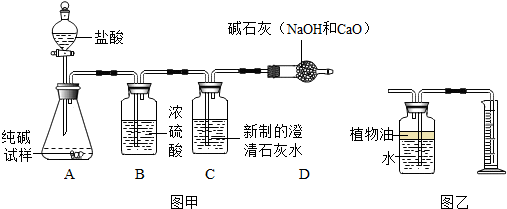
能用来制备和收集二氧化碳的装置是( )
| A、①和② | B、①和④ |
| C、②和④ | D、②和⑤ |
下列各组溶液,不另用任何外来试剂就能能鉴别出来的是( )
| A、Na2CO3 H2SO4 HCl KNO3 |
| B、NaOH NaCl MgCl2 HCl |
| C、HCl AgNO3 HNO3 MgCl2 |
| D、K2SO4 Na2CO3 BaCl2 HCl |
下列说法正确的是( )
| A、生铁的含碳量比钢低 |
| B、磷在氧气里燃烧时会产生大量白雾 |
| C、H2和O2的混合气体点燃时一定会爆炸 |
| D、在硫酸铜溶液中滴加氢氧化钠溶液能观察到蓝色絮状沉淀 |
以下关于铁的叙述,错误的是( )
| A、生铁和钢都是铁元素的单质 |
| B、铁是电和热的导体 |
| C、铁制品在潮湿的空气中会生锈 |
| D、铁丝能在氧气中燃烧 |