0 125658 125666 125672 125676 125682 125684 125688 125694 125696 125702 125708 125712 125714 125718 125724 125726 125732 125736 125738 125742 125744 125748 125750 125752 125753 125754 125756 125757 125758 125760 125762 125766 125768 125772 125774 125778 125784 125786 125792 125796 125798 125802 125808 125814 125816 125822 125826 125828 125834 125838 125844 125852 211419
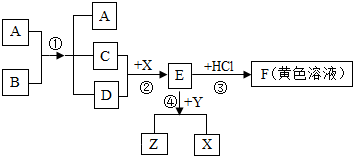
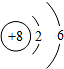 ,Y 有毒,X 是常见的金属单质.
,Y 有毒,X 是常见的金属单质.