0 125477 125485 125491 125495 125501 125503 125507 125513 125515 125521 125527 125531 125533 125537 125543 125545 125551 125555 125557 125561 125563 125567 125569 125571 125572 125573 125575 125576 125577 125579 125581 125585 125587 125591 125593 125597 125603 125605 125611 125615 125617 125621 125627 125633 125635 125641 125645 125647 125653 125657 125663 125671 211419
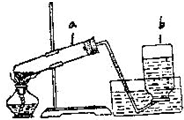 如图是实验室制取氧气的错误装置图:
如图是实验室制取氧气的错误装置图: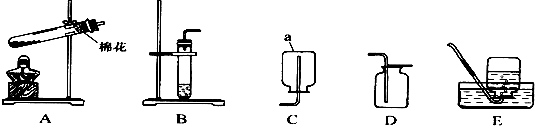
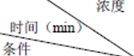



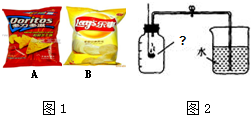 实验室里,张老师带领化学兴趣小组一起探究膨化食品(如图)包装袋内气体的成分.现有A、B两种膨化食品,请你一起参与他们的讨论并回答以下问题.
实验室里,张老师带领化学兴趣小组一起探究膨化食品(如图)包装袋内气体的成分.现有A、B两种膨化食品,请你一起参与他们的讨论并回答以下问题.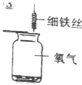 写出该反应的实验现象及文字表达式:
写出该反应的实验现象及文字表达式: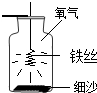 点燃后的铁丝能在氧气中燃烧,于是小兰设计了如图所示的装置进行实验探究,请你结合实验过程回答下列问题.
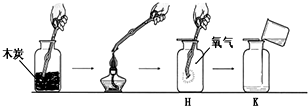
点燃后的铁丝能在氧气中燃烧,于是小兰设计了如图所示的装置进行实验探究,请你结合实验过程回答下列问题. 如图是铁丝、硫分别在氧气中燃烧的实验.请回答下列问题:
如图是铁丝、硫分别在氧气中燃烧的实验.请回答下列问题: