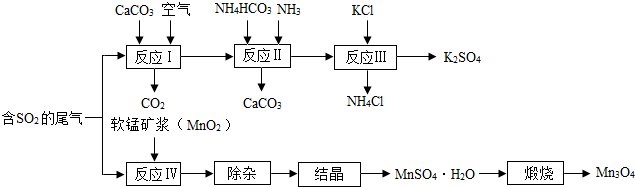
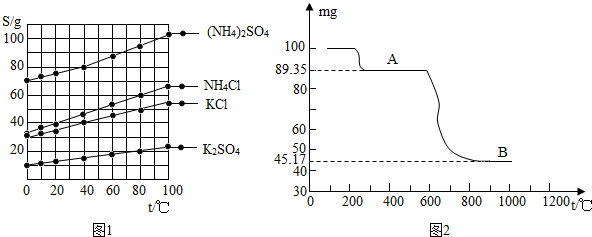
下列物质的转化能实现的是( )
A、H2SO4
| ||
B、CO
| ||
C、Cu(OH)2
| ||
D、NaNO3
|
下列关于H2、H2S、NH3、H2CO3四种物质的叙述中正确的是( )
| A、氢元素都以化合物形式存在 |
| B、氢元素的化合价都相同 |
| C、都含有氢分子 |
| D、都含有氢元素 |
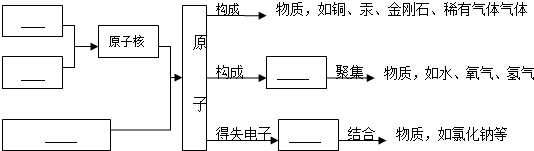
原子是构成物质的基本粒子.下列有关原子的叙述不正确的是( )
| A、原子的质子数等于核外电子数 |
| B、氧气、水、二氧化碳等物质中都含有氧元素,其中氧原子核内质子数都为8 |
| C、在化学变化中,原子的核电荷数和核外电子数都不发生改变 |
| D、原子质量主要集中在原子核上 |
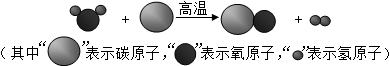
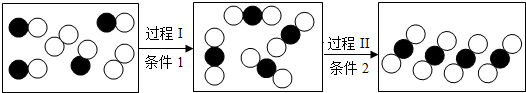
某密闭容器中,物质变化过程的微观示意图如图所示,图中“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子.下列说法正确的是( )
”代表氧原子.下列说法正确的是( )
 ”代表碳原子,“
”代表碳原子,“ ”代表氧原子.下列说法正确的是( )
”代表氧原子.下列说法正确的是( )
| A、过程Ⅰ反应类型化合反应 |
| B、过程Ⅱ发生了化学变化 |
| C、示意图中所有物质均为混合物 |
| D、参加反应的CO与O2分子个数比为1:1 |
下列过程中分子没有改变的是( )
| A、甲烷燃烧 | B、制蒸馏水 |
| C、电解水 | D、过氧化氢分解 |
与OH-具有相同质子数和电子数的微粒是( )
| A、HF |
| B、H2O |
| C、NH3 |
| D、NH2- |
关于Fe、Fe2+、Fe3+的说法中,正确的是( )
| A、他们结合其他原子的个数相同 |
| B、他们的质子数相同 |
| C、他们的最外层电子数相同 |
| D、他们的核外电子数相同 |