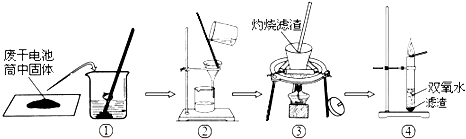
某气体由氢气、一氧化碳、甲烷中的一种或几种组成.点燃该气体后,在火焰上方罩一干冷烧杯,烧杯内壁出现水雾.把烧杯迅速倒转过来,注入少量澄清石灰水并振荡,石灰水变浑浊.下列对该气体组成的推断不正确的是( )
(已知:一氧化碳燃烧生成二氧化碳,甲烷完全燃烧生成二氧化碳和水)
(已知:一氧化碳燃烧生成二氧化碳,甲烷完全燃烧生成二氧化碳和水)
| A、符合的气体组成有四种情况 |
| B、不可能只含有一氧化碳 |
| C、可能只含有氢气和一氧化碳 |
| D、可能三种气体都存在 |
下列装置或操作能达到实验目的是( )
A、 实验室制取并收集O2 |
B、 点燃酒精灯 |
C、 检查装置气密性 |
D、 利用排空法收集CO2 |
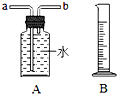
下列制取和收集气体的方案,可以直接采用如图所示装置进行的是( )


| A、用H2O2和MnO2制取收集O2 |
| B、用CaCO3和稀硫酸制取收集CO2 |
| C、用KMnO4制取收集O2 |
| D、用Zn粒和稀盐酸制取收集H2(难溶于水) |