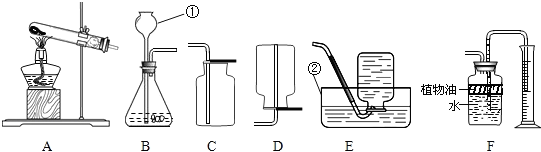
实验是学习化学的重要手段之一.某班同学分成两个小组,利用右下图所示装置进行如下实验,请你参与他们的实验过程.
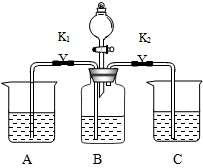
(1)第一小组同学的实验:
| 位置 | A | B | C | 分液漏斗 |
| 药品 | 澄清石灰水 | 碳酸钠溶液 | 澄清石灰水 | 稀盐酸 |
| 操作 | 关闭K1,打开K2和分液漏斗的活塞,缓慢滴加稀盐酸 | |||
| 现象,并写出 C中反应的化学方程式 | ______ | |||
| 操作 | 关闭K2,打开K1 | |||
| 现象 | B中液体沿导管流入A中,A中有白色沉淀产生 | |||
| 上述现象产生的原因 | ______ | |||
| 位置 | A | B | C | 分液漏斗 |
| 药品 | X溶液 | 稀盐酸 | 水(滴有石蕊溶液) | 碳酸钠溶液 |
| 操作 | 关闭K1,打开K2和分液漏斗的活塞,缓慢滴加碳酸钠溶液 | |||
| 现象 | ______ | |||
| 操作 | 关闭K2,打开K1 | |||
| 现象 | B中液体沿导管流入A中, A中有无色气体产生 | |||
| 写出A中X溶液的溶质 | ______ (至少写两种) | |||
在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
| 加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升(t)/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
如用______mL(填“10mL”、“50mL”或“100mL”)量筒量取水时,面对刻度线,仰视读数,则所配制的溶液______10%(填“=”、“>”或“<”)
(2)试绘出溶液的温度与加入盐酸的体积之间的变化关系曲线.

(3)根据曲线讨论溶液温度变化的原因.
①加入盐酸的量在2mL~10mL之间时:______.
②加入盐酸的量在10mL~20mL之间时:______.
(4)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?
答:______.
(5)在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因而无法确定盐酸与氢氧化钠是否恰好完全反应.为了证明这两种物质是否恰好完全反应,从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是得出“两种物质已恰好完全中和”的结论.
①你认为此结论是否正确?______,理由是______;
②写出该中和反应的化学方程式______;
③请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
| 实验方法 | 可能观察到的现象 | 结论 |
在一密闭容器内有X、Y、Z、Q四种物质,在一定条件下反应一定时间,测得反映前后各物质的质量如下表:
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 20 | 20 | 20 | 20 |
| 反应后质量/g | 20 | 30 | 16 | 14 |
- A.该反应一定是分解反应
- B.X是该反应的催化剂
- C.参加反应的Z、Q的质量比为2:3
- D.Z、Q的相对分子质量比一定为7:8
在一定条件下,下列物质在密闭容器内反应一段时间,测得反应前后各物质的质量如下:
| 物 质 | X | Y | Z | W |
| 反应前质量(g) | 10 | 2.2 | 16.2 | 0.9 |
| 反应后质量(g) | a | 4.4 | 8.1 | 1.8 |
- A.反应中Y、W两种物质变化的质量比为22:9
- B.a=15
- C.X、Z是反应物,Y、W是生成物
- D.Z为化合物
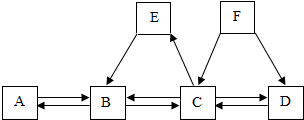 几种常见物质之间的相互转化关系如图所示(部分反应物和生成物及反应条件已略去).已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成;E为红色固体,与稀硫酸反应得到黄色溶液.下列有关判断正确的是
几种常见物质之间的相互转化关系如图所示(部分反应物和生成物及反应条件已略去).已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成;E为红色固体,与稀硫酸反应得到黄色溶液.下列有关判断正确的是