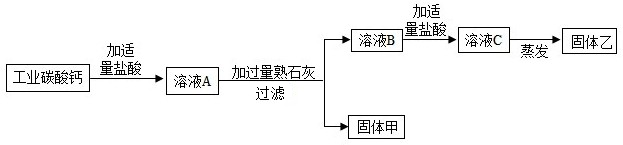
通过近一年的化学实验探究,小林发现金属和酸反应生成氢气的速率与金属的状态、酸的浓度、反应的温度等条件有关.下表是他对铝与稀盐酸反应受哪些条件的影响的探究(其中铝和稀盐酸每次的用量都相同).请你根据表中的信息填空:
| 实验编号 | 温度 | 铝的规格 | 盐酸浓度 |
| ① | 20℃ | 铝片 | 5% |
| ② | 20℃ | 铝片 | 10% |
| ③ | 铝粉 | 10% | |
| ④ | 30℃ | 铝片 | 5% |
(2)用②和③来探究铝的状态对反应速率的影响,小林进行实验③时的温度为______;
(3)要探究温度对反应速率的影响,小林设计的实验组合是______(填写实验编号);
(4)小林设计实验组合①②的目的是______;
(5)实验探究时,小林每次收集的氢气均为30mL,则实验中他还应记录的实验数据是______;
(6)在进行上述铝与稀盐酸反应时,粗心的小林不小心将氢氧化钠溶液倒入了铝片中,发现也有气泡产生,好奇的他继续进行了如下实验探究:
【提出问题】铝与氢氧化钠溶液反应时生成的气体是什么?
【进行猜想】猜想①:可能是CO2;猜想②:可能是O2;猜想③:可能是H2.
你认为猜想______是不合理的,理由是______;
【实验方案】①收集气体:实验时气体收集的方法是______;
②检验气体:验证猜想②的方法是______;
【得出结论】铝与氢氧化钠溶液反应的方程式为:
2Al+2NaOH+2H2O=2______+3H2↑(在横线上填上化学式).
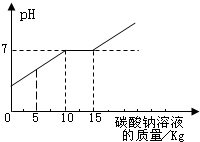 取盐酸与氯化钙的混合溶液11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液.所得溶液pH与加入的碳酸钠溶液的质量关系如图所示
取盐酸与氯化钙的混合溶液11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液.所得溶液pH与加入的碳酸钠溶液的质量关系如图所示 SO2 ②2CO+O2
SO2 ②2CO+O2 小魔术“空瓶生烟”方法如右图:上瓶中充满氯化氢气体,下瓶中充满氨气,抽开毛玻璃片,瓶中产生浓浓的白烟.发生的化学反应的微观过程可用下图表示:
小魔术“空瓶生烟”方法如右图:上瓶中充满氯化氢气体,下瓶中充满氨气,抽开毛玻璃片,瓶中产生浓浓的白烟.发生的化学反应的微观过程可用下图表示:
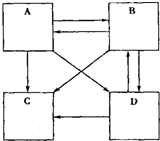 构建知识网络是一种重要的学习力法,如图是张南同学画出的四种物质之间的转化关系.图 中A、B、C、D四个方框,分别是碳酸钠溶液、氢氧化钠溶液、硝酸钠溶液和硫酸钠溶液四种溶液中的一种,图中方框之间的“→”表示某种物质能和其他物质反应生成箭头所指的物质.请回答下列问题:
构建知识网络是一种重要的学习力法,如图是张南同学画出的四种物质之间的转化关系.图 中A、B、C、D四个方框,分别是碳酸钠溶液、氢氧化钠溶液、硝酸钠溶液和硫酸钠溶液四种溶液中的一种,图中方框之间的“→”表示某种物质能和其他物质反应生成箭头所指的物质.请回答下列问题: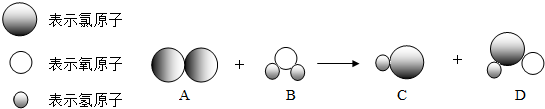
 TiCl4+2X,试推断X的化学式为
TiCl4+2X,试推断X的化学式为