单晶硅是重要的半导体材料,是我市的拳头产品,我市某厂生产的单晶硅曾用于制造我国的第一颗人造卫星.在硅及相关产品的生产中排放的废水含有HCl.该厂化验员对本厂排放废水中HCl的质量分数进行测定:将20毫升废水(假定其密度为1克/厘米3)样品置于锥形瓶中,用质量分数为1%的氢氧化钠溶液进行中和,共用去氢氧化钠溶液8克(假设废水中不含其他能与氢氧化钠溶液反应的物质).
(1)计算该废水中含HCl的质量分数.
(2)该厂每天产生废水100吨,若直接排放将对环境造成污染,必须进行无害化处理后才能进行排放,现准备用氢氧化钙粉末或质量分数为10%的氢氧化钠溶液进行中和.有关数据如下表所示:
| 物质 | 物质(或溶质)的相对分子质量 | 市场参考价(元/吨) |
| 氢氧化钙粉末 | 74 | 200 |
| 10%的氢氧化钠溶液 | 40 | 100 |
你将选择______(写化学式)来中和废水中的HCl,请说明理由______.
为了测定石灰石样品中碳酸钙的质量分数,甲、乙两同学分别进行了如下实验(杂质不溶于水且不参加反应).
甲同学进行的实验与所得数据如下:(每次取用的石灰石质量相同,稀盐酸的质量分数也相同)
| 实验 | 第一次 | 第二次 | 第三次 |
| 取用石灰石的质量/g | m | m | m |
| 取用稀盐酸的质量/g | 30 | 60 | 90 |
| 反应后过滤得到固体的质量(已干燥)/g | 6 | 2 | 1 |
①称取质量为W1g的石灰石样品,放入烧杯中;
②在烧杯中加入40g稀盐酸,充分搅拌,有气泡产生;
③充分反应后过滤、干燥,称得固体质量为W2g;
④______.
请你分析与计算:
(1)甲同学实验中碳酸钙的质量分数______.
(2)完成乙同学实验④中的步骤与预期现象______,该实验步骤的目的是______.
(3)比较甲、乙同学实验方案,你认为______(填“甲同学”或“乙同学”)方案较好,理由是______.
(4)求甲同学所用稀盐酸的溶质质量分数.(数据精确到0.1%)
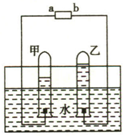 如图是电解水的简易装置,回答下列问题:
如图是电解水的简易装置,回答下列问题: