某同学测定的下列数据中,不合理的是( )
| A、用10mL的量筒量取7.5mL的水 |
| B、测得某粗盐中氯化钠的质量分数为90.5% |
| C、用pH试纸测得某河水的pH为5.2 |
| D、用托盘天平称量某固体质量为16.7g |
下列实验设计能达到实验目的是( )
| 选项 | A | B | C | D |
| 实 验 设 计 | 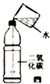 | 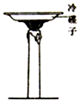 | 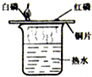 |  |
| 实验目的 | 验证二氧化碳与水反应生成碳酸 | 确定石蜡成分中含有碳元素 | 探究可燃物燃烧需要氧气和温度达到着火点 | 证明铁生锈是水和氧气共同作用的结果 |
| A、A | B、B | C、C | D、D |
小明要称量5克食盐进行实验,在称量过程中他发现指针指向右边(小明在称量过程中操作都正确),此时应该( )
| A、调节平衡螺母 | B、移动游码 |
| C、减少砝码 | D、增加食盐 |
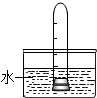 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究: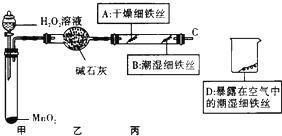 全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一.下面是对铁的腐蚀条件及铁锈组成的探究.
全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一.下面是对铁的腐蚀条件及铁锈组成的探究.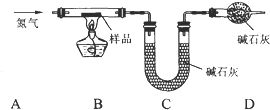
 某同学为研究可燃物的燃烧条件,他查阅资料得知:白磷着火点为40.C,红磷着火点为240.C,它们在空气中燃烧都会生成刺激呼吸道的白烟-五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验.
某同学为研究可燃物的燃烧条件,他查阅资料得知:白磷着火点为40.C,红磷着火点为240.C,它们在空气中燃烧都会生成刺激呼吸道的白烟-五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验.


