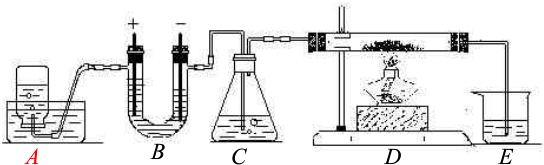
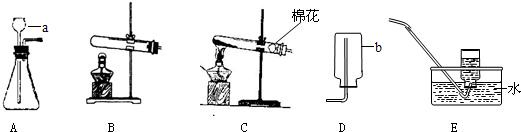
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
[查阅资料]
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
②生产原理反应(2):NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物.
③氯化铵分解的化学方程式是NH4Cl NH3↑+HCl↑.
NH3↑+HCl↑.
④部分生产流程如图所示: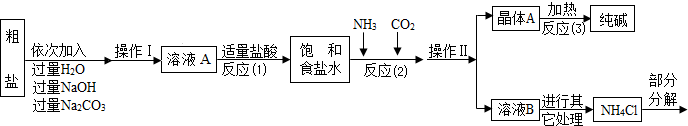
[问题讨论]
(1)①溶液A中的溶质有NaCl和______、______,②操作Ⅱ的名称为______.
③流程中NaOH溶液的作用是除去粗盐中的______.
④写出加入Na2CO3溶液所发生反应的化学方程式______.
(2)上述生产流程中可循环使用的是______(填序号).
A.CO2 B.NH3 C.HCl D.NaOH
[组成探究一](3)①晶体A受热分解的化学方程式为______.
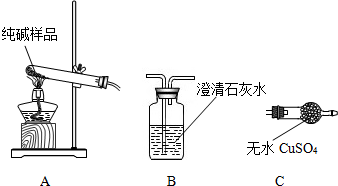
②设计实验检验纯碱样品中是否混有晶体A,请完成下表:
| 选择的装置 | 实验现象 | 实验结论 |
| ______ | ______ | 样品不含晶体A |
[组成探究二](4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为______,由此确定纯碱样品含有杂质NaCl.
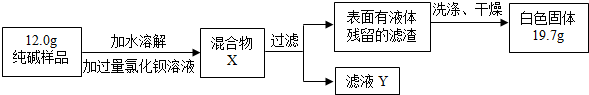
[组成探究三](5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
①判断加入氯化钡溶液是否过量的合适方法是______,然后观察现象判断.
A.静置混合物X,向上层清液中再滴少许氯化钡溶液 B.向滤液Y中滴加少许氯化钡溶液
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加______,然后观察现象判断.
A.氯化钡溶液 B.稀硫酸 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数为______(写出计算过程.4分)
[Mr(BaCl2)=208 Mr(Na2CO3)=106 Mr(BaCO3)=197Mr(NaCl)=58.5].