实验室可用KClO3和MnO2的固体混合物加热制取氧气.现取30.5g的固体混合物加热一段时间收集到一定质量的氧气后,停止反应.
(1)欲求得氧气的质量,将试管中的剩余物冷却到室温后,通过向该试管分多次加水测定剩余物质的办法求得.加水的质量与剩余固体的质量见下表:(MnO2不溶于水)
| 编号 | 1 | 2 | 3 | 4 |
| 加水的质量(g) | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 14.5 | 8.1 | m | 6 |
(2)为了测定固体混合物中MnO2的质量分数,需用______方法回收MnO2.
实验结束后,有3位同学分别展示了所测MnO2的质量分数.
| 小东 | 小南 | 小西 | |
| MnO2% | 35% | 10% | 15% |
①小东:称量KClO3和MnO2固体混合物时将固体放在天平的右边(1g以下用砝码)
②小东:滤液浑浊就干燥
③小东:烧杯里的物质还未充分溶解就开始过滤
④小南:称余下固体时只在天平的左盘垫了张纸
⑤小西:称余下固体前,部分固体洒落地下
(3)若要证明MnO2是该反应的催化剂,还需补做两个实验:①证明MnO2在反应前后化学性质不变.
②证明MnO2能改变KClO3反应放出氧气的速率.完成②需选用下图装置中的(填序号)______.要比较产生O2的快慢,除可以直接观察气泡产生的快慢,还可以______.
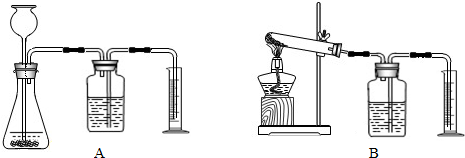
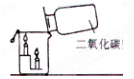 如图所示,点燃两只蜡烛.沿烧杯壁向烧杯内倾倒二氧化碳.
如图所示,点燃两只蜡烛.沿烧杯壁向烧杯内倾倒二氧化碳. 甲型H1N1流感病毒正威胁着人类的健康和安全.“达菲”(C16H28O4N2)是目前世界上治疗H1N1流感病毒的良药.生产“达菲”的主要原料是莽草酸,可从茴香中提取.回答下列问题:
甲型H1N1流感病毒正威胁着人类的健康和安全.“达菲”(C16H28O4N2)是目前世界上治疗H1N1流感病毒的良药.生产“达菲”的主要原料是莽草酸,可从茴香中提取.回答下列问题: