金属用途广泛,其结构和性质等是化学的重要研究内容.
(1)如图1是铝的原子结构示意图.下列说法不正确的是 .
| A.铝原子在反应中易得电子 |
| B.在化合物中铝通常显+3价 |
| C.铝是地壳中含量最多的金属元素 |
| D.铝可作导线是由于它具有良好的导电性 |
[提出问题]溶液A中的溶质可能有哪些?
[作出猜想]①只有Zn(NO3)2②Zn (NO3)2、Cu(NO3)2 ③Zn (NO3)2、NaNO3
[交流讨论]合理的猜想是 (填标号),其理由是 .
[实验探究]通过以下实验可确定固体B的成分,请将表填写完整.
| 实验步骤 | 现 象 | 有关反应的化学方程式 |
| 取固体B少量,滴加 | 有气泡产生 | (或 ) |
(4)黄铜(Cu﹣Zn合金)20g与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为119.6g.计算稀硫酸中溶质的质量分数(计算结果精确到0.1%)
(9分)化学与健康——从化学的视角看食品添加剂。
从化学的视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化等方面来研究。结合表中信息回答下列问题。
| 物质的组成与性能 | 用于食品添加剂 | |||
| 物质名称 | 物质组成 | 主要化学性质及在体内变化 | 类别或作用 | 法律规定 |
| 碳酸氢钠 | NaHCO3 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 | 膨松剂 | 可用 |
| 铁 (还原性铁粉) | Fe | 比较活泼的金属,能与胃酸反应 | 抗氧化剂 | 依据国家标准可用 |
| 食盐 | NaCl | 易溶、中性,与硝酸银溶液反应生成白色沉淀 | 调味剂 | 可用 |
| 甲醛 | CH2O |  | 防腐 | 国家严禁使用 |
| 亚硝酸钠 | NaNO2 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 | 发色剂、防腐剂 | 严格依据国家标准 |
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为 。
(3)碳酸氢钠是面食类食品经常使用的添加剂,如蒸馒头时人们常常加适量的碳酸氢钠,其作用是 ,写出发生反应的化学方程式 。
(4)亚硝酸钠(NaNO2)外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生。有一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠
(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可)。
(5)从改善食品的色香味、延长食品的保质期等方面,食品添加剂确实提高了现代食品的品质,但副作用也是显而易见的。我们需要食品添加剂吗?你的观点是 。
在学习化学的过程中,及时对所学知识进行整理,是一种好的学习方法。以下连线对应不正确的是
| A.相似物质(或微粒)之间的区别 | B.化学元素与人体健康 |
 |  |
| C.环境问题及对策 | D.化肥与植物生长 |
 |  |



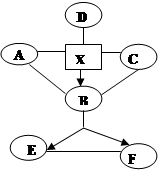
 ”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络:
”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络: