如表提供了在一定条件下.水能否与一些金属发生反应的信息.
如表提供了在一定条件下.水能否与一些金属发生反应的信息.
| 物质 | 钠与冷水 | 镁与冷水 | 镁与水蒸汽 | 铁与冷水 | 铁与水蒸气 |
| 能否发生反应 | 剧烈反应 | 缓慢反应 | ________ | 不反应 | 加热条件下能反应 |
②铁与水蒸气在加热条件下生成四氧化三铁和氢气.反应的化学方程式为________;
③铁虽然常温下与水不反应,但铁制品在潮湿的环境中容易生锈.某同学进行了如图所示实验.一周以后发现铁钉表面锈蚀.图中a、b、c三处锈蚀情况最严重的是________(填字母),由此可知常温下铁生锈的实质是铁与空气中的________ 和________共同作用的结果.请写出一种防止铁制品生锈的具体措施________.
学习了金属的性质之后,同学们决定用实验对铁、铝、铜三种金属的活动性顺序进行验证.
[实验一]将粗细相同的铁丝、铝丝、铜丝分别插入相同的稀盐酸中:
| 操作 | 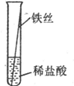 | 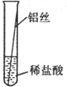 | 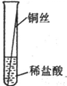 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
[反思评价]若不认真分析现象可能导致错误的结论.
[实验二]为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中,欲通过实验现象得出金属活动性顺序.
实验过程中能看到:硫酸铝溶液中的铁丝表面________,硫酸铜溶液中的铁丝表面________,反应的化学方程式________.
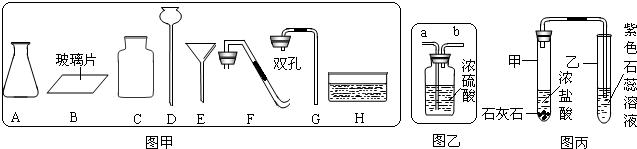
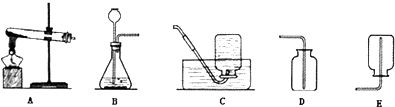
实验室常用下列装置来制取氧气:
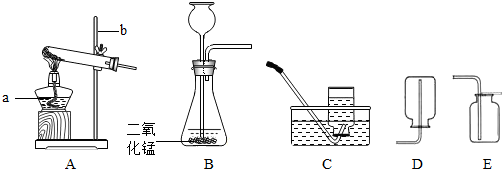
(1)写出图中有标号仪器的名称:a______、b______;
(2)用氯酸钾制取氧气时,发生反应的文字表达式为______.
(3)实验室常用氯化铵固体与碱石灰固体混和加热来制取氨气.常温下氨气是一种无色、有刺激
性气味的气体,密度比空气小,极易溶于水.制取并收集氨气时,应该从上图中选择的发生装置是______,收集装置是______.
(4)用E装置收集氧气时,检验氧气是否集满的方法是______.
(5)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是______(填序号),其中二氧化锰
起______作用,该反应的文字表达式为______.对此实验,让我们继续思考并研究几个问题:
问题①:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
我的实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化锰( MnO2 )粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间(t) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 |
问题②:过氧化氢(H2O2)溶液的浓度对反应速率有没有影响?你的实验方案是:______
问题③:还有哪些因素可能影响该反应的速率呢?请说出你的一个猜想:______.
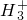 ,该粒子是
,该粒子是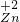 SO4
SO4