海洋资源十分丰富.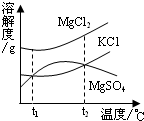
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、过滤、______可制得精盐.上述过程所用的主要玻璃仪器有:a烧杯、b玻璃棒、c______、d______.
(2)晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,图是它们的溶解度曲线示意图.设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则它们的大小关系为______.
(3)目前世界上60%的镁是从海水中提取的.其主要步骤如下:
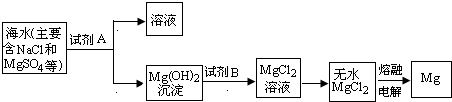
①提取Mg的过程中,试剂A可以选用______,试剂B选用______,
由无水MgCl2制取Mg的化学反应方程式为______.
②镁是重要的金属材料,广泛应用于合金、火箭和飞机制造业,世界上大部分镁是从海水中提取的.某校学习小组的同学对家乡附近海水中镁元素的含量进行测定.称取海水100kg,然后再加入足量的试剂A,过滤、洗涤、干燥后称量得到沉淀质量见下表(重复实验三次).
| 实验序号 | 第一次实验 | 第二次实验 | 第三次实验 |
| 所取海水质量/kg | 100 | 100 | 100 |
| 生成沉淀质量/kg | 0.28 | 0.29 | 0.30 |
③分离出Mg(OH)2后的NaCl溶液中还含有杂质CaCl2、Na2SO4,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液和Na2CO3溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl2溶液是为了除去______;加入过量Na2CO3溶液的目的是______.
(4)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是______.海底矿产资源“可燃冰”,其主要成分是水合甲烷晶体(CH4?nH2O),若水合甲烷晶体中CH4的质量分数为10%,则水合甲烷晶体的化学式为______.
为研究二氧化锰、加热对过氧化氢分解的影响,某同学设计了如下实验:
| 实验步骤(夹持固定装置已略去) | A、B、C三支试管中分别盛有等体积5%的过氧化氢溶液,如下图所示进行实验.仪器a的名称是__________,C中用于加热仪器的名称是_________.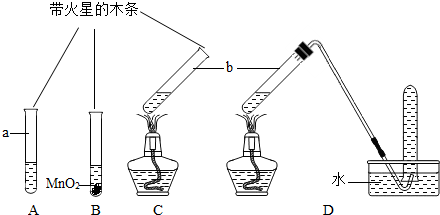 |
| 实验现象 | A:试管壁有气泡附着,带火星的木条不复燃. B:有大量气泡产生,带火星的木条复燃. C:有大量气泡产生,带火星的木条不复燃. D:有大量气泡产生,用带火星的木条检验收集的气体,木条复燃. |
| 分析 | B试管中发生反应的化学方程式是______________. 实验结束后仪器b中的液体质量都减少,原因是_____________________ ________________________________________________________________. |
| 结论 | ①分析A、B实验可以得出的结论是:______________________________. ②加热__________(填“能”或“不能”)促进过氧化氢分解产生氢气. |
某化工厂排出的废水中,阳离子可能含有Cu2+、Al3+、Mg2+中的一种或几种,阴离子可能含有Cl-、CO32-、OH-中的一种或几种,小平同学对该废水进行探究.
(1)观察废水呈显无色、透明、澄清的液体.
(2)取少量废水于试管中,加入一定量的NaOH溶液,看到有白色沉淀产生.
查阅有关资料:
材料1:Mg(OH)2、MgCO3是既不溶于水也不溶于碱的白色固体
材料2:Al(OH)3是白色固体,不溶于水、CO2的水溶液、也不溶于氨水;但Al(OH)3能溶于NaOH溶液生成NaAlO2和水.往NaAlO2溶液中通入CO2会产生Al(OH)3沉淀.
从(1)可得废水中阳离子不可能含有______,阴离子不可能含有______.
并对(2)的白色沉淀的组成进一步的探究.
提出猜想:
猜想1:白色沉淀只有Al(OH)3 猜想2:______ 猜想3:______
设计实验方案:
①取少量的白色沉淀于试管中,加入过量的NaOH溶液,观察到白色沉淀不溶解,证明了猜想______不成立.
②为了验证到底是上述哪种猜想,取①中的上层清液继续实验,请完成下表
| 操作 | 现象 | 结论 |
| ______ | ______ | ______ |
| ______ | ______ |
通过上述实验得到启示:要除去废水中的Al3+、Mg2+,不能用NaOH溶液,但可以往废水里加入过量的______除去,经处理后得到的废水可以用来灌溉农田,补充______(填“氮肥、磷肥、钾肥”).
 空气是一种宝贵的自然资源,请结合相关知识回答下列问题:
空气是一种宝贵的自然资源,请结合相关知识回答下列问题: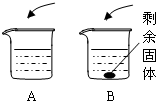 A、B两烧杯中均盛有100克水,分别加入不同质量的同种固体物质,用玻璃棒搅拌使其充分溶解,现象如图所示.此时,________烧杯中的溶液一定是该温度下的饱和溶液.
A、B两烧杯中均盛有100克水,分别加入不同质量的同种固体物质,用玻璃棒搅拌使其充分溶解,现象如图所示.此时,________烧杯中的溶液一定是该温度下的饱和溶液.