某化学实验小组在实验室用加热大理石(CaCO3)分解的方法制取生石灰(CaO).加热一段时间后,同学们对大理石是否分解提出怀疑.小组同学经研究决定对加热容器内剩余固体的成分进行探究,以证明大理石是否分解.请你参与探究.
实验限选的试剂:稀盐酸、蒸馏水、二氧化碳.
提出问题:加热大理石(CaCO3)后残留的固体成分是什么?
作出猜想:
猜想1:残留固体是CaCO3
猜想2:残留固体是CaO
猜想3:残留固体是________.
设计实验,按要求完成下表:
| 实验步骤 | 预期的实验现象与结论 |
| 步骤1:取少量残留固体于试管中,加入一定量的 ②,振荡充分溶解,静置. | 若完全溶解,则说明原残留固体是③.若部分溶解,则原残留固体可能是④. |
| 步骤2:若步骤1中有未溶固体,则取上层清夜少许于试管中,通入CO2. | 若⑤则说明原残留固体中含有CaO,否则不含CaO. |
| 步骤3:若步骤1中有未溶固体,向该固体中加入⑥. | 若有气泡产生,则原残留固体中含有⑦.否则只含有⑧. |
在课堂中,同学们用硫酸、硝酸钡、氢氧化钠、碳酸钾四种物质的溶液,进行复分解反应发生条件的探究.
(1)通过判断上述四种溶液两两之间能否发生反应,写出其中符合下列条件的化学方程式.
有沉淀生成的反应:______.
(2)下面图1是HCl和NaOH在水中解离的微观示意图;图2是稀盐酸和氢氧化钠反应的微观过程示意图.
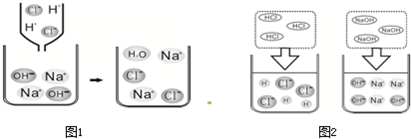
①盐酸和氢氧化钠发生反应的微观实质是什么?______.
②通过课堂上的探究能发现:在溶液中,除了H+和OH-不能大量共存外,______(填两种离子符号)也不能大量共存.
(3)利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.
①经测定,该溶液显酸性.则该溶液中一定含有的离子是______.(至少写4种离子符号)
②为验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证.(验证一种离子即可)
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| ______ | ______ |