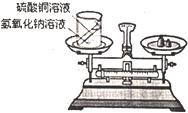
 在学习了质量守恒定律后,小明和小华来到实验室,他们用右图所示的实验装置,验证了氢氧化钠溶液和硫酸铜溶液反应是符合质量守恒定律的.
在学习了质量守恒定律后,小明和小华来到实验室,他们用右图所示的实验装置,验证了氢氧化钠溶液和硫酸铜溶液反应是符合质量守恒定律的.
(1)请写出该反应的化学方程______.
(2)实验结束后,在整理仪器时小明发现,原来氢氧化钠溶液是放在敞口容器中.于是他们对刚刚完成的实验产生了疑问:
[提出问题]①氢氧化钠是否变质;②如果氢氧化钠溶液儿经变质,“变质”的氢氧化钠与硫酸铜溶液反应为什么仍然符合质量守恒定律.
[查找资料]部分铜盐的溶解性表(20℃)
| 阳离子\阴离子 | SO42- | N03- | PO43- | Cl- | C032- |
| Cu2+ | 溶 | 溶 | 不 | 溶 | 不 |
[设计实验]怎样确定氢氧化钠是否变质?
| 实验过程 | 实验现象 | 结论 |
| ______ | ______ | ______ |
______.
②“变质”的氢氧化钠溶液与硫酸铜溶液反应,为什么仍然符合质量守恒定律:
______.
下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为______g.
(3)欲从海水中获得氯化钠晶体,应采取______方法.
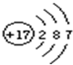 此元素为Cl 它属________元素(填金属或非金属)在化学反应中容易_________个电子变成离子,形成的离子用符号表示为________.
此元素为Cl 它属________元素(填金属或非金属)在化学反应中容易_________个电子变成离子,形成的离子用符号表示为________. 3CO+CO2+5H2O,则X的化学式是________.
3CO+CO2+5H2O,则X的化学式是________.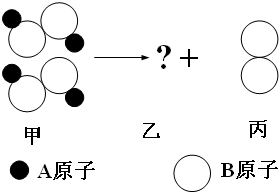 如图所示,每两个甲分子反应后生成两个乙分子和一个丙分子,已知甲、乙、丙分别为不同种类的纯净物,则乙物质的化学式为
如图所示,每两个甲分子反应后生成两个乙分子和一个丙分子,已知甲、乙、丙分别为不同种类的纯净物,则乙物质的化学式为