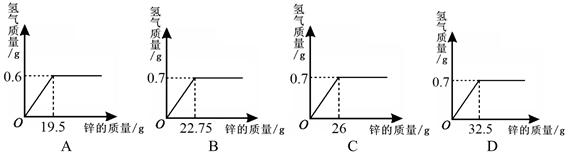
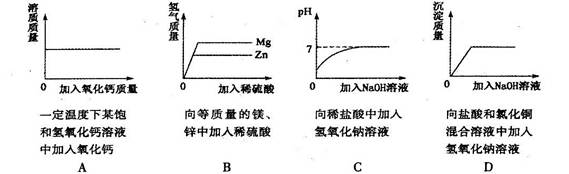
某氢氧化钠样品长时间暴露在空气中,经测定其主要成分为 Na2CO3 和 NaOH。将 7.3g 该样品加入盛有 100g 质量分数为 7.3%稀盐酸的烧杯中,再向其中加入 20g 质量分数为 10%的氢氧化钠溶液使过量的盐酸恰好完全中和,最后将所得溶液蒸干,此时得到固体的质量是
| A.5.85g | B.2.925g | C.5g | D.11.7g |
向10g部分变质了的烧碱固体中,加入73g溶质质量分数为10%的稀盐酸,恰好完全反应,则反应后溶液中溶质的质量为
| A.11.7g | B.5.85g | C.10g | D.4g |
—定量某Fe203样品(含有少量的Fe0、CuO),与100g9.8%的稀硫酸,恰好完全反应。该Fe2O3样品中氧元素的质量是
| A.0.8 g | B.1.6g | C.3.2 g | D.6.4 g |
有一包“铁”的粉末,可能含有Fe 、Fe2O3 Fe3O4中的一种或几种,现称取23.2g放在试管中,通入足量的一氧化碳并加热充分反应,将生成的气体全部通入足量的澄清石灰水,共得到40g的碳酸钙固体。关于这包“铁” 的粉末成分判断正确的是
| A.一定是纯净物 | B.一定有Fe 、Fe2O3Fe3O4三种 |
| C.如果有Fe ,就一定有Fe2O3 | D.如果有Fe2O3,就一定有Fe3O4 |
把一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.8 |
| 反应后质量(g) | 5.2 | X | 7.2 | 2.8 |
C.X=2.0g D. 该反应是化合反应
如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )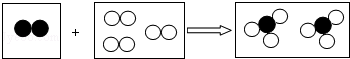
| A.该反应属于分解反应 |
| B.反应物和生成物中只有一种单质 |
| C.反应中共有两种元素参与 |
| D.参加反应的两种物质分子个数之比为2:3 |
已知某反映的微观示意图如下,下列说法正确的是( )
| A.该反应不符合质量守恒定律 | B.参加反应的分子个数比是5:2 |
| C.该反应中反应物都是化合物 | D.该反应前后的分子种类改变 |
在反应A+B=C+D中,20g A和10g B恰好完全反应,生成5g C,若要制得5g D,则需要B的质量为( )
| A.5g | B.4g | C.2g | D.3g |