以下是某实验小组在探究金属化学性质过程中的部分实验记录,请你根据记录回答下列问题.
| 金属 | 铝片 | 锌片 | 铁片 | 铜片 | 银片 |
| 盐酸 | 5% | W | 5% | 5% | 5% |
| 实验现象 | 开始无气泡,过一段时间后缓慢出现气泡,然后速度逐渐加快 | 产生气泡且速度较快 | 产生气泡但速度缓慢 | 无气泡 | 无气泡 |
(2)你认为在本实验中与锌片反应的盐酸的质量分数W应该是______.
(3)实验小组同学认为,用下列两组试剂都可以完成铜与银的金属活动性强弱的比较:
A.铜片与AgNO3溶液; B.银片与Cu(NO3)2溶液.
若你来做该实验,所选用的一组试剂是______(选填字母),相应的实验现象或反应的化学方程式是:______.
 碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.
碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.
(1)提出问题:黑色固体是什么?
(2)猜想与假设:黑色固体可能是:①______;②可能是炭粉;③可能是炭粉和氧化铜的混合物.请你补充猜想①.作出这些猜想的依据是______.
(3)实验方案:他们称取了2.22g碱式碳酸铜在试管中高温加热使之完全分解,冷却至室温,称得黑色固体产物的质量为1.6g.
(4)实验反思:①甲同学经过思考后,认为可以排除猜想③,理由是______(用化学方程式表示).
②乙同学根据质量守恒定律:化学反应前后,元素的种类和质量都不变.通过对得到的数据进行计算,排除了猜想②,他的理由是(通过计算式说明)______.
(5)实验结论:结合甲、乙同学的探究和查阅资料,丙同学确认只有猜想①成立.
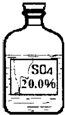
(6)实验拓展:丙同学想进一步探究该黑色固体的化学性质.他发现实验室有一瓶无色溶液,其标签严重破损(如图),老师告诉他该瓶试剂是硫酸、硫酸钠或硫酸镁溶液中的一种.他通过查阅资料得知常温下这三种物质的溶解度如下表:
| 物 质 | H2SO4 | Na2SO4 | MgSO4 |
| 常温下的溶解度∕g | 与水以任意比互溶 | 18.0 | 39.0 |
(1)填写下列表格:
| ① | ② | |||||
| 化学符号 | O | 2H2O | Al3+ | ______ | ______ | ______ |
| 名称或意义(只写一种) | ______ | ______ | ______ | 2个金原子 | 两个硫酸根离子 | 氧化铁中铁元素显+3价 |
元素周期律是学习和研究化学的重要工具.下表是元素周期表的部分信:
| 1H 氢 | 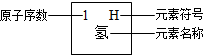 | 2He 氦 | ||||||
| 3Li 锂 | 4Be 铍 | 5B 硼 | 6C 碳 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 | |
| llNa 钠 | 12Mg 镁 | 13A1 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | XC1 氯 | 18Ar 氩 | |
| 19K 钾 | 20Ca 钙 | … | ||||||
(1)地壳中含量最多的元素的原子序数是______;
(2)分析上表规律,可推知,表中X=______;
(3)
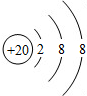 表示的是(写粒子符号)______.
表示的是(写粒子符号)______.(4)写出一个由1、7、8、16号四种元素组成的化合物的化学式______.
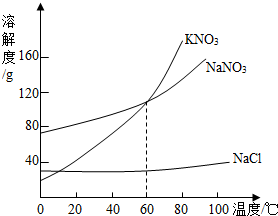 KNO3、NaNO2、NaCl三种固体物质的溶解度曲线如右图所示,回答下列问题:
KNO3、NaNO2、NaCl三种固体物质的溶解度曲线如右图所示,回答下列问题: