题目内容
对浓硫酸泄漏事故处理的讨论.
(1)小聪同学认为,如果仅用水稀释,并不能消除事故所造成的污染.因为从溶液的角度看,在稀释过程中溶质的 没变,仅仅是 变小了.
小明同学受到启发,制订了如下方案:
(2)小敏同学认为,小明同学的方案虽然有效,但有一个缺陷: .
(3)请你参照小聪的设计方案,结合小明的看法,也设计一个方案,并写出有关的化学方程式. .
(1)小聪同学认为,如果仅用水稀释,并不能消除事故所造成的污染.因为从溶液的角度看,在稀释过程中溶质的
小明同学受到启发,制订了如下方案:
| 采取措施 | 依据原理 | 效果评价 | 反应类型 |
| 向硫酸所流经范围抛撒大量氢氧化钠小颗粒 | 硫酸与氢氧化钠反应 | 将硫酸转化为无害物质,可消除污染 |
(3)请你参照小聪的设计方案,结合小明的看法,也设计一个方案,并写出有关的化学方程式.
考点:浓硫酸的性质及浓硫酸的稀释,中和反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)溶液加水稀释后,溶质的质量不变,溶液的质量分数变小;用氢氧化钠中和硫酸发生了中和反应,根据化学方程式的书写方法写出反应的方程式,注意配平和条件;
(2)根据浓酸和浓碱都有腐蚀性进行解答;
(3)根据实验目的,要选择没有腐蚀性的物质来中和浓硫酸.
(2)根据浓酸和浓碱都有腐蚀性进行解答;
(3)根据实验目的,要选择没有腐蚀性的物质来中和浓硫酸.
解答:解:(1)溶液加水稀释后,溶质的质量不变,溶液的质量分数变小;用氢氧化钠中和硫酸发生了复分解反应,化学方程式为2NaOH+H2SO4═Na2SO4+2H2O;
(2)浓酸和浓碱都有腐蚀性,如果氢氧化钠过量,也会造成污染.
(3)根据实验目的,要选择没有腐蚀性的物质来中和浓硫酸,故可以用氢氧化钙来中和硫酸.
故答案为:(1)质量;溶质质量分数;
(2)氢氧化钠也有强腐蚀性,如果氢氧化钠用量把握不准又可能引发新的污染;
(3)向硫酸所流经范围抛散大量氢氧化钙粉末;Ca(OH)2+H2SO4═CaSO4+2H2O.
(2)浓酸和浓碱都有腐蚀性,如果氢氧化钠过量,也会造成污染.
(3)根据实验目的,要选择没有腐蚀性的物质来中和浓硫酸,故可以用氢氧化钙来中和硫酸.
故答案为:(1)质量;溶质质量分数;
| 采取措施 | 依据原理 | 效果评价 | 反应类型 |
| 向硫酸所流经范围抛撒大量氢氧化钠小颗粒 | 硫酸与氢氧化钠反应 | 将硫酸转化为无害物质,可消除污染 | 复分解反应 |
(3)向硫酸所流经范围抛散大量氢氧化钙粉末;Ca(OH)2+H2SO4═CaSO4+2H2O.
点评:本题结合社会实际,通过浓硫酸的对性质的考查,培养了同学们判断能力和解决问题的能力,有一定的难度.

练习册系列答案
相关题目
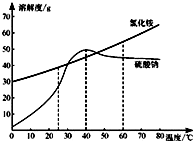 如图为氯化铵和硫酸钠的溶解度曲线.请回答:
如图为氯化铵和硫酸钠的溶解度曲线.请回答:

 用如图的装置来测定空气中氧气的体积分数
用如图的装置来测定空气中氧气的体积分数 请根据如图所示,回答下列问题:
请根据如图所示,回答下列问题: 按要求完成下列小题:
按要求完成下列小题: