题目内容
10.某葡萄糖注射液中溶质质量分数为15%.180g葡萄糖完全氧化,可以产生2804kJ的热量.医生给某病人注入了500mL(密度为1g/mL)该葡萄糖注射液,这些葡萄糖完全氧化后共产生多少热量?分析 先计算500mL(密度为1g/mL)15%的葡萄糖溶液中葡萄糖的质量,再根据每180g葡萄糖完全氧化可以产生2804kJ的热量计算所含葡萄糖能放出的热量.
解答 解:500mL(密度为1g/mL)15%的葡萄糖溶液中葡萄糖的质量=500mL×1g/mL×15%=75g,完全氧化可以产生的热量=$\frac{75g}{180g}×2804kJ$=1168.3kJ.
故答案为:这些葡萄糖完全氧化后共产生1168.3kJ的热量.
点评 本题涉及了能量的相互转化以及简单的化学计算,解答时注意隐含条件“180g葡萄糖完全氧化,可以产生2804kJ的热量”的利用,是解答此题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.小军同学在学习酸碱盐有关知识时,对一些沉淀物质的颜色产生了兴趣.老师告诉他氢氧化铜是蓝色、氢氧化铁是红褐色,让他自己探究氢氧化亚铁的颜色.下面请你和他一起探究.
【查阅资料】
(1)铁有两种氢氧化物,它们可以分别由相对应的可溶性盐与碱溶液反应而制得.
(2)氢氧化亚铁在空气中立即被氧化.
(3)硫酸铜溶液是蓝色,硫酸亚铁溶液是浅绿色.
【提出猜想】:氢氧化亚铁是浅绿色.
【实验过程】:在2支试管里分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察现象.请补充完成表:
【学习交流】(1)氢氧化亚铁是白色而不是浅绿色.
(2)小军联系到CO2与C的反应,认为FeCl3溶液可以转化为FeCl2溶液.你认为小军的理由是单质的铁也可以将FeCl3还原成FeCl2.
【查阅资料】
(1)铁有两种氢氧化物,它们可以分别由相对应的可溶性盐与碱溶液反应而制得.
(2)氢氧化亚铁在空气中立即被氧化.
(3)硫酸铜溶液是蓝色,硫酸亚铁溶液是浅绿色.
【提出猜想】:氢氧化亚铁是浅绿色.
【实验过程】:在2支试管里分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察现象.请补充完成表:
| FeCl3溶液 | FeSO4溶液 | |
| 滴入NaOH溶液的现象 | 生成红褐色沉淀 | 先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色沉淀. |
化学方程式 | 基本反应类型属于复分解反应 | FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 4Fe(OH)2+2O2+H2O=4Fe(OH)3↓ |
(2)小军联系到CO2与C的反应,认为FeCl3溶液可以转化为FeCl2溶液.你认为小军的理由是单质的铁也可以将FeCl3还原成FeCl2.
 观察铁生锈的实验:
观察铁生锈的实验: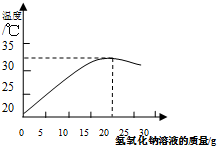 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)