题目内容
6.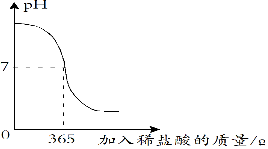 草木灰是植物燃烧后的残余物,草木灰中几乎含有植物体内所有的矿质元素.草木灰的主要成分是碳酸钾,干木柴烧出来的草木灰pH值为12左右且无任何杂质.某化学兴趣小组取来干木柴燃烧后产生的草木灰69g,并向其中加入稀盐酸进行反应.实验过程中的pH图象如图所示,求:
草木灰是植物燃烧后的残余物,草木灰中几乎含有植物体内所有的矿质元素.草木灰的主要成分是碳酸钾,干木柴烧出来的草木灰pH值为12左右且无任何杂质.某化学兴趣小组取来干木柴燃烧后产生的草木灰69g,并向其中加入稀盐酸进行反应.实验过程中的pH图象如图所示,求:(1)当溶液为中性时,加入稀盐酸的质量为365g.
(2)计算实验所用的稀盐酸的溶质质量分数.
分析 碳酸钾和稀盐酸反应生成氯化钾、水和二氧化碳,根据反应的化学方程式和碳酸钾的质量可以计算恰好完全反应时消耗的氯化氢的质量,进一步可以计算实验所用的稀盐酸的溶质质量分数.
解答 解:(1)由图中数据可知,当溶液为中性时,加入稀盐酸的质量为365g.
故填:365.
(2)设溶液为中性时,消耗氯化氢质量为x,
K2CO3+2HCl═2KCl+H2O+CO2↑,
138 73
69g x
$\frac{138}{69g}$=$\frac{73}{x}$,
x=36.5g,
实验所用的稀盐酸的溶质质量分数为:$\frac{36.5g}{365g}$×100%=10%,
答:实验所用的稀盐酸的溶质质量分数为10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.甲、乙是化学中常见的两种固体物质,它们的溶解度曲线如图,则下列有关说法错误的是( )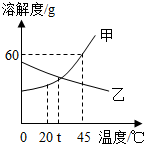

| A. | t℃时,甲、乙的溶解度相等 | |
| B. | 蒸发溶剂和升高温度可以使不饱和的甲溶液变为饱和溶液 | |
| C. | 45℃时,50g甲放入100g水中可以形成150g溶液 | |
| D. | 若甲物质中含有少量的乙物质,可采用降温结晶法提纯甲物质 |
1.在20世纪70年代,人们把信息、材料和能源誉为当代文明的三大支柱;而80年代以高技术群为代表的新技术革命,又把新材料、信息技术和生物技术并列为新技术革命的重要标志.这都充分说明了材料对人类的重要性.下列不属于有机合成材料制成的物品的是( )
| A. | 塑料水杯 | B. | 涤纶外套 | C. | 木头娃娃 | D. | 橡胶雨鞋 |
18.分析推理是一种重要的研究和学习的方法,下列分析推理中正确的是( )
| A. | 原子是构成物质的微粒,因此所有物质都是由原子构成的 | |
| B. | 中和反应有水生成,因此有水生成的反应一定是中和反应 | |
| C. | 物质燃烧时会伴随着发光发热的现象,因此有发光发热的现象发生时,一定有物质在燃烧 | |
| D. | 化合物是由不同的元素组成的纯净物,因此由不同的元素组成的纯净物一定都是化合物 |
15.学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题.从化学的角度看,下列说法中不正确的是( )
| A. | 夜晚发现液化气泄漏是不能开灯检查的 | |
| B. | 人们每天的饮食中都应有蔬菜、水果,其目的是补充蛋白质 | |
| C. | 扑灭电器、图书档案等火灾最适宜的灭火器是液态二氧化碳灭火器 | |
| D. | 含硫的煤不完全燃烧时,排放出污染环境的气体是SO2和CO |
16.老年人体缺钙易引发的病症是( )
| A. | 贫血 | B. | 夜盲症 | C. | 骨质疏松 | D. | 甲状腺肿大 |
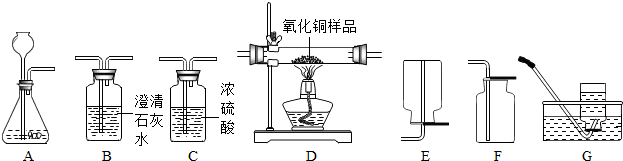
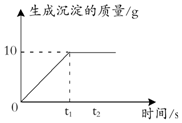 在某次实验过程中,某兴趣小组收集到10g一氧化碳和二氧化碳的混合干燥气体.为了测定混合气体中一氧化碳的质量,该小组将混合气体通入足量的澄清石灰水中,实验所得的数据如图所示.求:
在某次实验过程中,某兴趣小组收集到10g一氧化碳和二氧化碳的混合干燥气体.为了测定混合气体中一氧化碳的质量,该小组将混合气体通入足量的澄清石灰水中,实验所得的数据如图所示.求: