题目内容
3.元素周期表是学习和研究化学的重要的工具,它的内容十分丰富.下表是元素周期表的部分内容,请回答下列问题:
(1)表中A的名称是磷,属于元素非金属(填“金属”或“非金属”);
(2)表中具有相对稳定结构的元素有He、Ne、Ar(填元素符号);
(3)表中不同种元素最本质的区别是B(填序号)
A.相对原子质量不同 B.质子数不同 C.中子数不同
(4)从表中查出地壳中含量最多的非金属元素的相对原子质量为16.00;
(5)与氧元素处于同一族的元素有硫(或S);
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:AB(填序号)
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
(7)图
 是某粒子的结构示意图,则该原子最外层电子数为2,该原子的元素位于第3周期,该微粒的符号为Mg2+.
是某粒子的结构示意图,则该原子最外层电子数为2,该原子的元素位于第3周期,该微粒的符号为Mg2+.
分析 (1)原子序数为15的元素为磷,写出名称即可;根据偏旁分析元素的种类;
(2)根据相对稳定结构与最外层电子数关系考虑;
(3)依据元素间的本质区别是质子数的不同分析判断;
(4)先弄清地壳中含量最多的非金属元素,再根据元素周期表的部分内容,查知其相对原子质量;
(5)根据同一纵行的元素属于同一族的元素,进行分析解答;
(6)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律;
(7)根据原子的核电荷数=核外电子数,元素的周期数与原子的电子层数有密切的关系;结合离子符号的书写写出该离子的符号.
解答 解:(1)原子序数为15的元素为磷,磷为“石”字旁,因此是固态非金属元素;故填:磷;非金属;
(2)最外层电子数为8(一个电子层最外层是2)属于相对稳定结构,所以表中具有相对稳定结构的元素是氦、氖、氩元素;故填:He、Ne、Ar;
(3)由所学以及元素周期表的信息可知元素间的本质区别是质子数的不同;故选项为:B;
(4)地壳中含量最多的非金属元素为氧元素;再根据元素周期表的内容,查知其相对原子质量为16.00;故填:16.00;
(5)同一纵行的元素属于同一族的元素,故与氧元素处于同一族的元素是硫元素;故填:硫(或S);
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:A.从左到右,各元素原子的电子层数相同;B.从左到右,各元素原子的原子序数依次增加;C、从左到右,各元素原子的最外层电子数增加;故填:AB;
(7)由微粒的结构示意图可知质子数=12,核外电子数=10,质子数>核外电子数,因此为镁离子,其离子符号为:Mg2+;镁离子是镁原子失去2个电子得到的,因此该元素的原子的最外层电子数是2;镁原子有3个电子层,因此位于第三周期;故填:2;3;Mg2+.
点评 本题考查学生根据元素周期表中所给信息解题的能力和有关化学用语的书写,难度不大.

| 物质 | 在氧气中点燃现象 | 反应文字表达式 |
| 木炭(黑、固) | 剧烈地燃烧,发出白光,放出大量的热,能生成使澄清石灰水变浑浊的气体 | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 |
| 石蜡(白、固) | 发出白光,瓶壁上有水雾,生成使石灰水变浑浊的气体 | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
| 铁丝(银白、固) | 剧烈燃烧,火星四射,放出大量的热,生成了黑色固体 | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |
1、从深海鱼油中提取出来的一种不饱和脂肪酸被称为“脑黄金”,它的化学式为C26H40O2,
它由三种元素组成,其中氢元素与氧元素的质量比为5:4.
2、人类生活和工农业生产都离不开水,请回答下列问题:
(1)自来水厂生产自来水时,没有使用的净水方法是蒸馏.
| A.沉淀 | B.过滤 | C.煮沸 | D.蒸馏 |
(3)自来水消毒过程中通常会发生如下反应,其反应的微观过程可用下图表示:
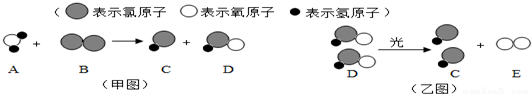
请回答以下问题:①以上物质中属于氧化物的是A (填序号).
②上述反应中属于分解反应的是乙(填“甲图”或“乙图”)
 .
. 为了探究“水的净化”过程,某实验小组从东昌湖某区域中取了水样,观察到:
为了探究“水的净化”过程,某实验小组从东昌湖某区域中取了水样,观察到: