题目内容
水是生命的源泉,也是不可缺少的资源.请你参与下列有关问题的讨论:
(1)自来水的生产过程大体如下:过滤池中有活性炭层,活性炭起 作用.处理水时,通常通入一定量氯气(或加入漂白粉),其作用是 .
(2)在实验室中要出去天然水中的固体杂质,可采用 的方法.
(3)长期饮用硬水对人体健康不利,要区分硬水和软水,可用 检验.现要降低水的硬度,在家庭里通常采用 的方法.
(4)在日常生活中硬水的危害有 .
(1)自来水的生产过程大体如下:过滤池中有活性炭层,活性炭起
(2)在实验室中要出去天然水中的固体杂质,可采用
(3)长期饮用硬水对人体健康不利,要区分硬水和软水,可用
(4)在日常生活中硬水的危害有
考点:自来水的生产过程与净化方法,过滤的原理、方法及其应用,硬水与软水,碳单质的物理性质及用途
专题:空气与水
分析:(1)根据活性炭可吸附色素和异味的物质,然后通入氯气或加入漂白粉消毒杀菌解答;
(2)根据自来水净化过程包括沉降、过滤、吸附、消毒等操作答,沉降用于除去大颗粒不溶物,过滤可除去不溶性固体杂质解答
(3)根据用肥皂水和区分硬水和软水解答;
(4)根据生活中常用硬水会使衣服洗不干净,锅炉内结垢浪费燃料甚至爆炸等危害.
(2)根据自来水净化过程包括沉降、过滤、吸附、消毒等操作答,沉降用于除去大颗粒不溶物,过滤可除去不溶性固体杂质解答
(3)根据用肥皂水和区分硬水和软水解答;
(4)根据生活中常用硬水会使衣服洗不干净,锅炉内结垢浪费燃料甚至爆炸等危害.
解答:解:
(1)过滤池中活性炭有吸附作用,能吸附色素和异味;通入一定量氯气(或加入漂白粉)的作用是消毒杀菌.故答案为:吸附,消毒杀菌.
(2)在实验室中过滤可除去天然水中的固体杂质,故答案为:过滤.
(3)用肥皂水和区分硬水和软水,要降低水的硬度,可用煮沸的方法.故答案为:肥皂水,煮沸.
(4)在日常生活中常使用硬水,会带来很多危害,例如用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.故答案为:用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.
答案:
(1)吸附,消毒杀菌
(2)过滤
(3)肥皂水 煮沸
(4)用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.
(1)过滤池中活性炭有吸附作用,能吸附色素和异味;通入一定量氯气(或加入漂白粉)的作用是消毒杀菌.故答案为:吸附,消毒杀菌.
(2)在实验室中过滤可除去天然水中的固体杂质,故答案为:过滤.
(3)用肥皂水和区分硬水和软水,要降低水的硬度,可用煮沸的方法.故答案为:肥皂水,煮沸.
(4)在日常生活中常使用硬水,会带来很多危害,例如用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.故答案为:用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.
答案:
(1)吸附,消毒杀菌
(2)过滤
(3)肥皂水 煮沸
(4)用硬水洗衣服既浪费肥皂也洗不净衣物,还会使衣服变硬等.
点评:本题综合考查自来水生产过程中的净水操作和目的,同时考查硬水的检验和生活中的危害.

练习册系列答案
相关题目
下列对“20℃时,硝酸钾的溶解度为31.6g”的解释正确的是( )
| A、20℃时,31.6g硝酸钾溶解在100g水中恰好饱和,则20℃时,硝酸钾的溶解度为31.6 |
| B、20℃时,100g溶液中含31.6g硝酸钾 |
| C、31.6g硝酸钾溶解在100g水中达到饱和状态 |
| D、20℃时,31.6g硝酸钾溶解在100g水中恰好达到饱和状态 |
下列各组物质相互混合后能形成溶液且溶剂不是水的是( )
| A、8mL酒精与2mL水混合 |
| B、1小粒碘投入2mL色拉油中 |
| C、1g铁粉投入一定量的稀硫酸中 |
| D、5mL汽油与10mL煤油混合 |
如图所示的四个图象,能正确反映对应变化关系的是( )
A、 水的电解 |
B、 木炭在密闭的容器内燃烧 |
C、 加热一定量的高锰酸钾制氧气 |
D、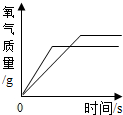 等质量的氯酸钾在有无二氧化锰条件下加热 |
“人造空气”帮助人类实现了“太空漫步”的梦想.“人造空气”中,N2的体积分数是70%,O2的体积分数在20%左右,还有CO2等其他气体.下列说法正确的是( )
| A、“人造空气”中氮气含量比空气中的氮气含量高 |
| B、燃着的蜡烛放入“人造空气”中会立刻熄灭 |
| C、带火星的木条在“人造空气”中不会复燃 |
| D、“人造空气”若只含有O2会更有益于人的呼吸 |