题目内容
20.铁锈的主要成分是Fe2O3,为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的盐酸中,他首先看到锈迹溶解,溶液呈黄色.这是因为(用化学方程式表示)Fe2O3+6HCl=2FeCl3+3H2O;不一会儿,又看到溶液中有有气泡产生的现象,这是因为(用化学方程式表示)Fe+2HCl=FeCl2+H2↑.分析 根据金属氧化物以及金属与酸的反应进行分析,铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁,其水溶液为黄色,铁能与盐酸反应生成氯化亚铁和氢气.
解答 解:
铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁,其水溶液为黄色,这是因为(用化学方程式表示)Fe2O3+6HCl=2FeCl3+3H2O;铁能与盐酸反应生成氯化亚铁和氢气,故不一会儿,又看到溶液中有有气泡产生的现象,这是因为(用化学方程式表示)Fe+2HCl=FeCl2+H2↑.
故答案为:
黄; Fe2O3+6HCl=2FeCl3+3H2O; 有气泡产生; Fe+2HCl=FeCl2+H2↑
点评 本题考查了铁锈以及铁与盐酸反应的实验现象和化学方程式的书写,完成此题,可以依据已有的知识进行,需要同学们在品是的学习中加强基础知识的储备,以便灵活应用.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
1.物质的性质决定它的用途.下列物质的性质与用途对应关系不正确的( )
| A. | 食醋具有酸性,可用于消除松花蛋中所含碱性物质的涩味 | |
| B. | 铁的活泼性比铝弱,铁制品比铝制品在空气中更耐腐蚀 | |
| C. | 磷燃烧能产生白烟,可用于制作烟幕弹 | |
| D. | 糖类氧化可以放出能量--做人类供能的食物 |
2.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
| D | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、洗涤干燥 |
| A. | A | B. | B | C. | C | D. | D |
5.下列物质的用途与物质化学性质无关的是( )
| A. | 用铜丝做导线 | B. | 用氮气充入灯泡可延长使用寿命 | ||
| C. | 用稀有气体作金属焊接保护气 | D. | 氧气可以供给呼吸 |
9.下列属于化学变化的是( )
| A. | 铁丝弯曲 | B. | 浓盐酸挥发 | C. | 燃放烟花 | D. | 干冰升华 |
10.下列结构示意图表示的元素在元素周期表中第二周期元素的是( )
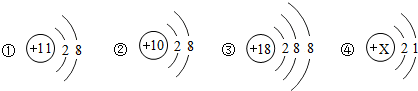
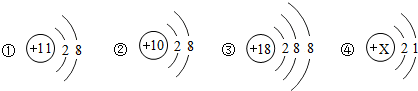
| A. | ①②④ | B. | ①② | C. | ②④ | D. | 无法判断 |
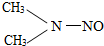 2013年震惊全国的复旦大学投毒案,使用剧毒化学物质N-二甲基亚硝胺(模型见图)该化学物质常温下呈黄色液体,中性,有弱臭味,粘滞度低,溶于水、乙醇、乙醚、二氯甲烷.侵入途径:摄入、吸入或经皮肤吸收,引起肝、肾损害甚至死亡.危险特性:遇明火、高热易燃.与强氧化剂可发生反应,受热分解放出有毒的一氧化氮烟气,还生成两种常见的碳氧化合物.
2013年震惊全国的复旦大学投毒案,使用剧毒化学物质N-二甲基亚硝胺(模型见图)该化学物质常温下呈黄色液体,中性,有弱臭味,粘滞度低,溶于水、乙醇、乙醚、二氯甲烷.侵入途径:摄入、吸入或经皮肤吸收,引起肝、肾损害甚至死亡.危险特性:遇明火、高热易燃.与强氧化剂可发生反应,受热分解放出有毒的一氧化氮烟气,还生成两种常见的碳氧化合物. 