题目内容
(8分)如图是实验室制取气体的常用装置,请回答下列问题.
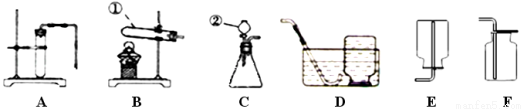
(1)写出图中标号仪器的名称① ;② 。
(2)检查装置A气密性的方法是 。
(3)某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,可以选择的气体发生装置是 (填字母),二氧化锰在反应中起 作用。装置C可以作为实验室用过氧化氢制取氧气的发生装置,它的优点是 。
(4)实验室用大理石与稀盐酸制取二氧化碳,制取装置可以选择 (填字母)。二氧化碳容易导致温室效应,结合实际你认为如何才能做到低碳生活 。
(1)①试管;②分液漏斗。
(2)将导管口放入水中,双手握住试管,观察导管口是否有气泡冒出。
(3)B,催化。可以控制化学反应速率。
(4)AF(或CF)。少乘私家车等(合理即可)。
【解析】
试题分析:(1)①为试管,②为长颈漏斗;(2)将导管口放入水中,双手握住试管,观察导管口是否有气泡冒出。(3)根据反应物状态和反应条件知,应选择固固加热型发生装置,二氧化锰其催化作用,装置C可以通过活塞控制化学反应速率。(4)根据反应物状态可以选择固液常温型发生装置,二氧化碳密度比空气大,可以用向上排空气法收集,故选AF或CF;要做到低碳,就必须减少二氧化碳的排放,如减少使用化石燃料,步行代替私家车,少使用一次性木筷等。
考点:气体的实验室制法,温室效应的防治。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案为了测定某铜、锌合金的组成,称取10g该合金粉末,在粉末中连续6次加入稀硫酸反应,每加一次稀硫酸,记录完全反应后所得剩余固体的质量,实验数据如下:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量(g)[ | 8.7 | 7.4 | 6.1 | 4.8 | 3.5 | 3.5 |
(注意:以下各题,只要求填写计算结果,不要求写计算过程)
(1)据表中数据,计算该合金中锌的质量为 ;
(2)计算所加稀硫酸的溶质的质量分数为 (精确到0.1%);
(3)计算恰好完全反应后所得溶液的溶质的质量分数为 (精确到0.1%)。
对下列现象的解释或者结论错误的是
A.“花香四溢”——分子在不断运动
B.过氧化氢分解——在化学变化中分子可以再分
C.铁制品表面刷漆——可防止生锈
D.伸入集气瓶中燃着的木条熄灭——瓶中气体一定是CO2
为确认氢氧化钠溶液与稀盐酸反应时,滴加的盐酸是否过量,取少量反应后的溶液于试管中,所用试剂及判断的方法不合理的是
实验方案 | 使用的试剂 | 判断的方法 |
A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
D | 紫色石蕊溶液 | 如果溶液变成红色,表明盐酸已经过量 |
