题目内容
18.下列除杂方法正确的是( )| A. | 用稀盐酸除去生石灰中的石灰石 | |
| B. | 用足量的水除去碳酸钙中的碳酸钠 | |
| C. | 用氢氧化钡除去硝酸钾中的硫酸铜 | |
| D. | 用氢氧化钾除去氢氧化钠中的碳酸钠 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、石灰石和生石灰均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的试剂错误.
B、碳酸钠易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的试剂错误.
C、硫酸铜能与氢氧化钡溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂正确.
D、碳酸钠不与氢氧化钾反应,不能除去杂质,故选项所采取的试剂错误.
故选:BC.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
9.保持氧气的化学性质的最小粒子是( )
| A. | 氧元素 | B. | 氧分子 | C. | 氧离子 |
6.通过下列实验得出结论,其中正确的是( )
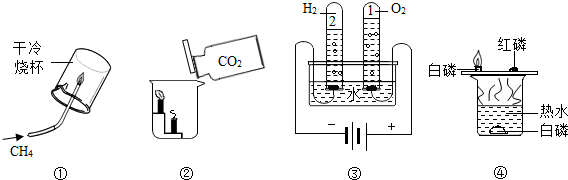
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③说明水是由氢、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低.

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③说明水是由氢、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低.
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
13.某校化学学习小组准备用生石灰制取氢氧化钠固体,他们进行如下探究过程.请根据他们的探究回答问题.
【查阅资料】
【设计实验、制取氢氧化钠】
步骤①:将一定量的生石灰加入一只洁净的烧杯中,加入碳酸钠溶液,充分反应.
步骤②:将所得的混合溶液冷却至室温.
步骤③:将冷却后的混合物过滤、洗涤、干燥得到固体A和溶液B.
(1)过滤操作中,除烧杯和玻璃棒外,过滤必须用到玻璃仪器是漏斗.
【提出问题、假设痏想】
(2)固体A中的成分是什么?
甲同学认为是:CaC03.
乙同学认为是:CaCO3和Ca(OH)2.
溶液B中溶质的成分是什么?
丙同学认为是:NaOH
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:NaOH、Na2CO3.
【验证猜想、实验探究】
(3)为了验证各自的猜想,甲、乙同学分别进行了实验:
【交流表达、反思评价】
(4)同学们经过讨论后认为,甲同学的实验不能(填“能”或“不能”)证明固体A的成分,理由是过量的稀盐酸能和氢氧化钙反应生成氯化钙和水,能和碳酸钙反应生成氯化钙、水和二氧化碳,最终同学们确定乙同学的猜想是正确的;
(5)同学们得到的固体A8.7g.加入足量的稀盐酸充分反应后.将溶液加热浓缩、蒸发结晶得到ll.lg固体,则固体A中所含的CaC03的质量是5g;
(6)同学们结合对固体成分的探究.经过讨论确定了丁同学对溶液B的猜想正确,理由是氢氧化钙是过量的.
【拓展延伸、巩固提高】
(7)同学们欲将溶液B加热浓缩,加热不久.溶液出现浑浊.只好停止加热.请解释加热时溶液出现浑浊的原因是氢氧化钙的溶解度随着温度升高而减小,加热时部分氢氧化钙析出,于是,同学们立即变换方案.向B溶液中加入适量的碳酸钠溶液.过滤,将滤液加热浓缩至饱和,降温、过滤、洗涤、烘干得到比较纯净的氢氧化钠固体.
【查阅资料】
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH 的溶解度 | 42 | 109 | 129 | 174 | 314 | 147 |
| Ca(OH)2 的溶解度 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
步骤①:将一定量的生石灰加入一只洁净的烧杯中,加入碳酸钠溶液,充分反应.
步骤②:将所得的混合溶液冷却至室温.
步骤③:将冷却后的混合物过滤、洗涤、干燥得到固体A和溶液B.
(1)过滤操作中,除烧杯和玻璃棒外,过滤必须用到玻璃仪器是漏斗.
【提出问题、假设痏想】
(2)固体A中的成分是什么?
甲同学认为是:CaC03.
乙同学认为是:CaCO3和Ca(OH)2.
溶液B中溶质的成分是什么?
丙同学认为是:NaOH
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:NaOH、Na2CO3.
【验证猜想、实验探究】
(3)为了验证各自的猜想,甲、乙同学分别进行了实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸 | 固体溶解,产生气泡 | 自己的猜想正确 |
| 乙同学:用一支洁净的试管取少量的固体A,加水,充分振荡.向上层清液中滴加 酚酞试液 | 上层清液由无色变为红色 | 自己的猜想正确 |
(4)同学们经过讨论后认为,甲同学的实验不能(填“能”或“不能”)证明固体A的成分,理由是过量的稀盐酸能和氢氧化钙反应生成氯化钙和水,能和碳酸钙反应生成氯化钙、水和二氧化碳,最终同学们确定乙同学的猜想是正确的;
(5)同学们得到的固体A8.7g.加入足量的稀盐酸充分反应后.将溶液加热浓缩、蒸发结晶得到ll.lg固体,则固体A中所含的CaC03的质量是5g;
(6)同学们结合对固体成分的探究.经过讨论确定了丁同学对溶液B的猜想正确,理由是氢氧化钙是过量的.
【拓展延伸、巩固提高】
(7)同学们欲将溶液B加热浓缩,加热不久.溶液出现浑浊.只好停止加热.请解释加热时溶液出现浑浊的原因是氢氧化钙的溶解度随着温度升高而减小,加热时部分氢氧化钙析出,于是,同学们立即变换方案.向B溶液中加入适量的碳酸钠溶液.过滤,将滤液加热浓缩至饱和,降温、过滤、洗涤、烘干得到比较纯净的氢氧化钠固体.
3.在20℃时,100g水中最多可溶解A物质50g;在60℃时,100g水中最多可溶解B物质100g,则A、B 两种物质的溶解度大小比较为( )
| A. | 无法比较 | B. | A=B | C. | A<B | D. | A>B |
7.向氯化铜溶液中加入过量铁粉,充分反应,过滤,滤纸上剩下的固体物质是( )
| A. | 铁 | B. | 铜 | C. | 氯化铜和铜 | D. | 铁和铜 |

 .
.