题目内容
 在21℃和充分搅拌下,将不同体积0.0365g/mL HCl溶液和未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下:
在21℃和充分搅拌下,将不同体积0.0365g/mL HCl溶液和未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下:
| 盐酸的体积V(mL) | 5.0 | 10.0 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 | 40.0 | 45.0 |
| NaOH的体积(mL) | 45.0 | 40.0 | 35.0 | 30.0 | 25.0 | 20.0 | 15.0 | 10.0 | 5.0 |
| 溶液温度t(℃) | 22.2 | 23.3 | 24.6 | 25.8 | 27.0 | 27.8 | 26.1 | 24.4 | 22.8 |
(2)据图可知V盐酸:VNaOH溶液=______时,两溶液恰好完全反应.
(3)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有______(填符号).
(4)在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.分析曲线变化的原因______.
解:(1)盐酸和氢氧化钠反应的方程式为:NaOH+HCl=NaCl+H2O,该反应是酸和碱发生的中和反应,属于复分解反应;
(2)从表格读出二者恰好完全反应时温度最高,此时盐酸是30ml,氢氧化钠是20ml,所以V盐酸:VNaOH溶液=30:20=3:2;
(3)当V盐酸:VNaOH溶液=1:4时,是氢氧化钠溶液过量.因此含有的微粒有氢氧化钠中的Na+、OH-、H2O,还含有产物氯化钠中提供的Cl-,故含有的微粒:Na+、OH-、Cl-、H2O;
(4)根据盐酸的体积与温度一一对应做出相应的点,再将点连成平滑的曲线.曲线趋势是先上升再下降,这样变化的原因是:中和反应伴随的能量变化是放热,随着盐酸的增加,温度逐渐升高,到恰好反应时温度最高;随着盐酸的继续滴加,过量的盐酸会吸收溶液的热量,所以温度又逐渐降低.
分析:根据表格给出的信息逐一分析:随着反应的进行,根据温度的变化,确定反应的程度及溶液中的微粒;
根据表格的数据描点,连线画出曲线图并利用中和反应伴随的能量变化进行分析变化的原因.
点评:本题考查学生的读取信息的能力,并用读取的信息完成相应的问题.
(2)从表格读出二者恰好完全反应时温度最高,此时盐酸是30ml,氢氧化钠是20ml,所以V盐酸:VNaOH溶液=30:20=3:2;
(3)当V盐酸:VNaOH溶液=1:4时,是氢氧化钠溶液过量.因此含有的微粒有氢氧化钠中的Na+、OH-、H2O,还含有产物氯化钠中提供的Cl-,故含有的微粒:Na+、OH-、Cl-、H2O;
(4)根据盐酸的体积与温度一一对应做出相应的点,再将点连成平滑的曲线.曲线趋势是先上升再下降,这样变化的原因是:中和反应伴随的能量变化是放热,随着盐酸的增加,温度逐渐升高,到恰好反应时温度最高;随着盐酸的继续滴加,过量的盐酸会吸收溶液的热量,所以温度又逐渐降低.

分析:根据表格给出的信息逐一分析:随着反应的进行,根据温度的变化,确定反应的程度及溶液中的微粒;
根据表格的数据描点,连线画出曲线图并利用中和反应伴随的能量变化进行分析变化的原因.
点评:本题考查学生的读取信息的能力,并用读取的信息完成相应的问题.

练习册系列答案
相关题目
在21℃和充分搅拌下,将不同体积0.0365g/mL HCl溶液和未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下:
(1)发生反应的化学方程式:______,该反应的基本类型是______.
(2)据图可知V盐酸:VNaOH溶液=______时,两溶液恰好完全反应.
(3)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有______(填符号).
(4)在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.分析曲线变化的原因______.

| 盐酸的体积V(mL) | 5.0 | 10.0 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 | 40.0 | 45.0 |
| NaOH的体积(mL) | 45.0 | 40.0 | 35.0 | 30.0 | 25.0 | 20.0 | 15.0 | 10.0 | 5.0 |
| 溶液温度t(℃) | 22.2 | 23.3 | 24.6 | 25.8 | 27.0 | 27.8 | 26.1 | 24.4 | 22.8 |
(2)据图可知V盐酸:VNaOH溶液=______时,两溶液恰好完全反应.
(3)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有______(填符号).
(4)在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.分析曲线变化的原因______.

 (2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题.
(2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题. 在21℃和充分搅拌下,将不同体积0.0365g/mL HCl溶液和未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下:
在21℃和充分搅拌下,将不同体积0.0365g/mL HCl溶液和未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下: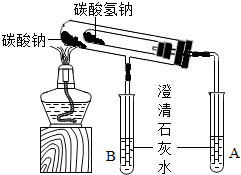 校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.
校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.