题目内容
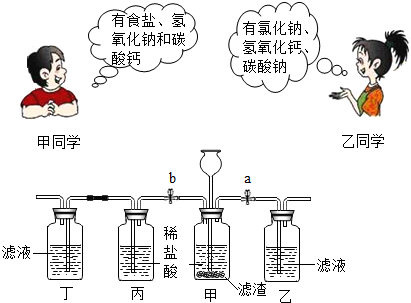
某实验小组将制作皮蛋的原料生石灰、纯碱和食盐放入水中,充分反应后过滤,得到澄清溶液.对该溶液的组成,甲、乙同学分别做出以下推测:
(1)我认为上述两位同学的推测都有不足,理由是
(2)我的推测是:该溶液中一定存在的溶质是
(3)为进一步确定该溶液所有可能的组成,同学们设计了如图所示的实验装置进行验证.
①甲装置中发生反应的化学方程式为
②关闭止水夹b,打开止水夹a,若观察到乙装置出现浑浊现象,则滤液中的溶质有
③关闭止水夹a,打开止水夹b,若观察到
④打开a和b,

(1)我认为上述两位同学的推测都有不足,理由是
甲同学的猜想中碳酸钙难溶于水,而乙同学的猜想中碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀
甲同学的猜想中碳酸钙难溶于水,而乙同学的猜想中碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀
.(2)我的推测是:该溶液中一定存在的溶质是
氢氧化钠和氯化钠
氢氧化钠和氯化钠
.(3)为进一步确定该溶液所有可能的组成,同学们设计了如图所示的实验装置进行验证.
①甲装置中发生反应的化学方程式为
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.②关闭止水夹b,打开止水夹a,若观察到乙装置出现浑浊现象,则滤液中的溶质有
NaCl、NaOH、Ca(OH)2
NaCl、NaOH、Ca(OH)2
.③关闭止水夹a,打开止水夹b,若观察到
丁中液面上升且有气泡产生
丁中液面上升且有气泡产生
,则滤液中含有的溶质为NaCl、NaOH、Na2CO3
NaCl、NaOH、Na2CO3
.④打开a和b,
丁中无气泡产生,乙中不变浑浊,结论滤液中只含NaCl和NaOH
丁中无气泡产生,乙中不变浑浊,结论滤液中只含NaCl和NaOH
(填写现象和结论).分析:(1)甲同学的猜想中碳酸钙难溶于水,而碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀,可以据此解答该题;
(2)所给的原料为生石灰、纯碱和食盐以及水,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙和氢氧化钠,所以此时过滤所得滤液中一定含有氢氧化钠和氯化钠,可以据此解答该题;
(3)①由题中信息可以知道,氧化钙可以和水反应,而生成的氢氧化钙可以和碳酸钠反应生成碳酸钙,所以在滤渣中含有碳酸钙,所以甲装置中发生的反应为盐酸和碳酸钙的反应;
②反应生成了二氧化碳,而二氧化碳能够使澄清石灰水变浑浊,可以据此解答该题;
③关闭止水夹a,打开止水夹b,产生的二氧化碳能把盐酸压入丁中,盐酸能与碳酸钠反应生成气体从而检验碳酸钠的存在,可以据此解答该题;
④同时打开a和b,则气体能进入乙,能将盐酸压入丁,若乙不变浑浊且丁无气泡,则证明只含有氯化钠和氢氧化钠,可以据此解答该题.
(2)所给的原料为生石灰、纯碱和食盐以及水,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙和氢氧化钠,所以此时过滤所得滤液中一定含有氢氧化钠和氯化钠,可以据此解答该题;
(3)①由题中信息可以知道,氧化钙可以和水反应,而生成的氢氧化钙可以和碳酸钠反应生成碳酸钙,所以在滤渣中含有碳酸钙,所以甲装置中发生的反应为盐酸和碳酸钙的反应;
②反应生成了二氧化碳,而二氧化碳能够使澄清石灰水变浑浊,可以据此解答该题;
③关闭止水夹a,打开止水夹b,产生的二氧化碳能把盐酸压入丁中,盐酸能与碳酸钠反应生成气体从而检验碳酸钠的存在,可以据此解答该题;
④同时打开a和b,则气体能进入乙,能将盐酸压入丁,若乙不变浑浊且丁无气泡,则证明只含有氯化钠和氢氧化钠,可以据此解答该题.
解答:解:(1)甲同学的猜想中碳酸钙难溶于水,而碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀,所以可以判断甲乙同学的猜想都有不足;
(2)氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙和氢氧化钠;根据反应可知,生成了氢氧化钠,氯化钠不参与反应,所以所得溶液中一定有氢氧化钠和氯化钠;
(3)①碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②关闭止水夹b,打开止水夹a,则产生的二氧化碳进入乙中,乙装置出现浑浊现象,说明溶液中含有氢氧化钙,所以溶液中含有的溶质为:NaCl、NaOH、Ca(OH)2;
③关闭止水夹a,打开止水夹b,产生的二氧化碳能把盐酸压入丁中,盐酸能与碳酸钠反应生成气体从而检验碳酸钠的存在,所以若观察到丁中液面上升且有气泡产生,则说明验证丁中滤液里含有碳酸钠;
④同时打开a和b,则气体能进入乙,且能将盐酸压入丁,若乙不变浑浊且丁无气泡,则证明只含有氯化钠和氢氧化钠.
故答案为:(1)甲同学的猜想中碳酸钙难溶于水,而碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀;
(2)氢氧化钠和氯化钠;
(3)①CaCO3+2HCl═CaCl2+H2O+CO2↑;
②NaCl、NaOH、Ca(OH)2;
③观察到丁中液面上升且有气泡产生;NaCl、NaOH、Na2CO3;
④丁中无气泡产生,乙中不变浑浊,滤液中只含NaCl和NaOH.
(2)氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙和氢氧化钠;根据反应可知,生成了氢氧化钠,氯化钠不参与反应,所以所得溶液中一定有氢氧化钠和氯化钠;
(3)①碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②关闭止水夹b,打开止水夹a,则产生的二氧化碳进入乙中,乙装置出现浑浊现象,说明溶液中含有氢氧化钙,所以溶液中含有的溶质为:NaCl、NaOH、Ca(OH)2;
③关闭止水夹a,打开止水夹b,产生的二氧化碳能把盐酸压入丁中,盐酸能与碳酸钠反应生成气体从而检验碳酸钠的存在,所以若观察到丁中液面上升且有气泡产生,则说明验证丁中滤液里含有碳酸钠;
④同时打开a和b,则气体能进入乙,且能将盐酸压入丁,若乙不变浑浊且丁无气泡,则证明只含有氯化钠和氢氧化钠.
故答案为:(1)甲同学的猜想中碳酸钙难溶于水,而碳酸钠和氢氧化钙反应生成难溶于水的碳酸钙沉淀;
(2)氢氧化钠和氯化钠;
(3)①CaCO3+2HCl═CaCl2+H2O+CO2↑;
②NaCl、NaOH、Ca(OH)2;
③观察到丁中液面上升且有气泡产生;NaCl、NaOH、Na2CO3;
④丁中无气泡产生,乙中不变浑浊,滤液中只含NaCl和NaOH.
点评:对常见的碱Ca(OH)2、常见的盐Na2CO3的性质必须烂熟于心,才能对灵活多变的题目应付自如.因此平时要多注意对基础知识的牢固掌握和对知识的灵活运用.

练习册系列答案
相关题目








