题目内容
4.甲图所示为测定空气中氧气含量的装置及药品.
(1)为获得较为准确的实验数据,下列做法不正确的是D.
A.检查装置的气密性
B.燃烧匙中的红磷足量
C.红磷熄灭,广口瓶冷却后打开弹簧夹
D.点燃红磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
(2)市售“暖宝宝”中发热剂主要成分是:铁粉、炭粉、水和食盐等,反应原理可简化为铁生锈.小明用配置的发热剂按图乙装置实验,测定出空气中氧气的体积分数.他不是将足量的发热剂堆在瓶底,而是将其涂抹在广口瓶内壁的四周,这样做的目的是增大与氧气的接触面积,加快缓慢氧化.他又用木炭代替红磷、但没能测定出空气中氧气的体积分数,其原因是木炭燃烧产生CO2,气压基本不变,在老师的指导下用氢氧化钠溶液代替水来做此实验,(已知氢氧化钠和氢氧化钙化学性质相似)也测定出空气中氧气的体积分数.依据以上信息可总结出二氧化碳不支持燃烧,可以与可溶性碱反应(化学性质).
分析 (2)本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.
保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数;
(2)暖宝宝暖宝宝中的铁粉与水和空气中氧气发生了缓慢氧化,进而放出热量;物质缓慢氧化会放出热量,氯化钠的作用是加速铁粉氧化,更快地放出热量.据此分析解答有关的问题.
解答 解:(1)保证实验成功的条件是:正式开始实验前,要先检查装置的气密性,防止装置漏气;燃烧匙中的红磷足量;等集气瓶冷却,打开止水夹;点燃红磷后燃烧匙插入集气瓶慢,塞紧瓶塞之前,瓶内部分空气受热逸出,进入的水的量应大于集气瓶体积的$\frac{1}{5}$;
(2)暖宝宝暖宝宝中的铁粉与水和空气中氧气发生了缓慢氧化,从而使瓶内的压强减小;将其涂抹在广口瓶内壁的四周,这样做的目的是增大与氧气的接触面积,加快缓慢氧化;木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化,所以实验失败;依据以上信息可总结出二氧化碳不支持燃烧,可以与可溶性碱反应.
答案:
(1)D;
(2)增大与氧气的接触面积,加快缓慢氧化;木炭燃烧产生CO2,气压基本不变;不支持燃烧,可以与可溶性碱反应.
点评 本题主要考查实验测定空气中氧气含量的原理及可能造成实验失败的原因的分析,理解实验的原理是解答本题的关键,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
15.如图所示操作中,正确的是( )
| A. | 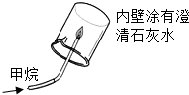 检验甲烷燃烧有CO2生成 | B. | 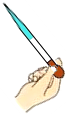 将带有残留夜的滴管倒持 | ||
| C. |  读液体体积 | D. |  吹灭酒精灯 |
12.下列有关氧气的叙述正确的是( )
| A. | 空气中氧气的质量约占21%,呼吸、燃烧、炼钢等都要用到氧气 | |
| B. | 空气中氧气含量的测定实验中,可以将红磷换成木炭 | |
| C. | 用含有氧元素的物质反应才有可能产生氧气 | |
| D. | 氧气的化学性质比较活泼,是可燃物 |
9.下列变化属于化学变化的是( )
| A. | 分离液态空气制氧气 | B. | 活性炭的吸附 | ||
| C. | 铁矿石炼铁 | D. | 酒精挥发 |
16.用托盘天平称取10.3g食盐,如果指针向左偏,应采取的措施是( )
| A. | 移动游码 | B. | 加适量砝码 | C. | 减少药品 | D. | 增加药品 |
13.下列实验操作中正确的是( )
| A. | 取用试剂后将滴管清洗再放回原瓶 | |
| B. | 可用燃着的木条鉴别氮气和二氧化碳 | |
| C. | 向燃着的酒精灯里添加酒精 | |
| D. | 试管可以直接加热 |
 如图为某微粒所属的元素在元素周期表中的相关信息,由此可知:
如图为某微粒所属的元素在元素周期表中的相关信息,由此可知: