题目内容
17.央视财经频道报道了深圳海砂楼 问题,根 据当地政府的调查结果显示,问题的根源就是建设时使用大量海砂.海砂中超标的氯离子将严重腐蚀建筑中的钢筋,使楼体不稳甚至倒塌.而与海砂相比,河砂则不含氯离子.家住海滨的小明想通过实验证明楼下的一堆砂子是不是海砂,除水外,下列四种药品中他还需要选择( )①BaCl2 ②AgNO3 ③HNO3 ④HCl.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ①② |
分析 根据题意,与海砂相比,河砂则一般不含氯离子,故检验楼下的一堆砂子是不是海砂,检验是否含氯离子即可,据此进行分析解答.
解答 解:与海砂相比,河砂则一般不含氯离子,故检验楼下的一堆砂子是不是海砂,检验是否含氯离子即可,检验氯离子可选用用硝酸酸化的硝酸银溶液,若产生白色沉淀,说明含有氯离子.
①氯离子不能与BaCl2溶液反应,不能用于检验是否含氯离子.
②氯离子与AgNO3溶液反应生成不溶于硝酸的氯化银白色沉淀,硝酸银溶液和硝酸可用于检验是否含氯离子.
③氯离子与AgNO3溶液反应生成不溶于硝酸的氯化银白色沉淀,硝酸银溶液和硝酸可用于检验是否含氯离子.
④氯离子不能与AgNO3溶液反应生成不溶于硝酸的氯化银白色沉淀,不能使用HCl,否则会引入氯离子,不能确定砂子中是否含有氯离子.
故②③可用于检验是否含氯离子.
故选:B.
点评 本题难度不大,掌握氯离子的检验方法(用硝酸酸化的硝酸银溶液)是正确解答本题的关键.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
7.下列实验操作正确的是(??)
| A. | 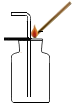 收集二氧化碳并验满 | B. | 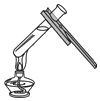 加热液体 | ||
| C. |  取用液体 | D. |  收集氧气 |
5.为了测定某碳酸钠样品(其中杂质为氯化钠)的质量分数,小明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.实验数据如下表:
根据上表内数据,完成下列有关计算:
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
12.化学反应A=B+C,若将agA在一定条件下充分反应生成bgB和cgC,下列关系式一定正确的是( )
| A. | a=b+c | B. | a≥b+c | C. | a≤b+c | D. | a<b+c |
3.下列说法中正确的是( )
| A. | 饱和溶液降温析出晶体后,溶质质量分数一定减小 | |
| B. | t℃某饱和的氢氧化钙溶液加入少量的生石灰,充分反应后,恢复到t℃,则溶液的质量不变 | |
| C. | 将密度为1.84 g/cm3溶质质量分数为98%的浓硫酸稀释为49%的硫酸,所加水的体积与所取浓硫酸的体积一定相等 | |
| D. | MgO与CuO的混合物与98g10%的稀硫酸恰好完全反应,则原混合物中氧元素的质量是1.6g |
4.在化学变化中必然会发生改变的是( )
| A. | 分子的种类 | B. | 原子的种类和数目 | ||
| C. | 原子核内的质子数 | D. | 原子的质量和性质 |
 ”、“
”、“ ”和
”和 ”分别表示三种不同的分子.试分析回答:
”分别表示三种不同的分子.试分析回答: