题目内容
15.对比归纳是学习化学的重要方法.请回答下列问题.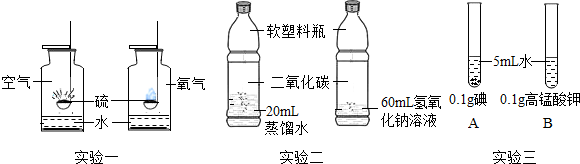
(1)实验一说明影响硫燃烧剧烈程度的因素是氧气的浓度.
(2)实验二用于证明二氧化碳和氢氧化钠能否反应,该实验设计不符合对比实验的基本原则,理由是取用两种液体的量不同.
(3)实验三观察到A中固体几乎不溶,B中固体全部溶解,说明影响物质溶解性的因素是溶质的种类.
分析 (1)根据氧气的浓度不同分析回答;
(2)根据液体的量不同分析;
(3)根据不同溶质的性质不同分析.
解答 解:(1)实验一中硫在氧气中燃烧比在空气中燃烧剧烈,说明影响硫燃烧剧烈程度的因素是氧气的浓度.
(2)实验二用于证明二氧化碳和氢氧化钠能否反应,该实验设计不符合对比实验的基本原则,理由是取用两种液体的量不同.
(3)实验三观察到A中固体几乎不溶,B中固体全部溶解,由于溶剂相同,溶质不同,说明影响物质溶解性的因素是溶质的种类.
故答为:(1)氧气的浓度;(2)取用两种液体的量不同;(3)溶质的种类.
点评 对比归纳是学习化学的重要方法,学会利用此方法来进行探究物质的性质,提高实验的能力.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
5.为防止食品变质,常在食品包装盒中放入一小袋用来吸收水分和氧气的物质是( )
| A. | 铁粉 | B. | 烧碱 | C. | 纯碱 | D. | 生石灰 |
7.阅读下面科普短文.
19世纪50年代,白磷火柴在欧洲普遍流行.19世纪末,人们发现利用白磷做火柴的工人,易患一种磷毒性颌骨坏死的疾病,至此白磷的毒性受到关注.各国也在不同时期宣布禁止生产和销售白磷火柴,于是火柴上的白磷渐渐被红磷取代.现代火柴头主要成分是氯酸钾和硫磺,火柴盒侧面的磷皮则使用了红磷,辅料包括石蜡、二氧化锰、炭黑、黏合剂和稳定剂等.
纯净的白磷是无色透明的晶体,遇光会逐渐变黄,因而又叫黄磷.白磷剧毒,误食0.1g就能致死.白磷接触皮肤也会引起吸收中毒.白磷不溶于水,易溶于二硫化碳.经测定,白磷的分子式为P4.
白磷最特殊的性质就是能在潮湿的空气中发生缓慢氧化,反应产生的部分能量以光能的形式放出,故在暗处可看到白磷发光.当缓慢氧化积累的能量达到它的着火点(40℃)时便发生自燃,因此白磷通常储存在水中.
白磷和红磷虽然一字之差,但是它们的结构、着火点和毒性却有很大不同.白磷是剧毒、着火点低、四面体型分子,而红磷是无毒、着火点较高、链状分子
依据上文,回答下列问题:
(1)白磷的物理性质无色固体(或不溶于水、易溶于二硫化碳等)(任写一条).
(2)白磷燃烧反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)现代火柴摩擦生火时燃烧的物质中,除木棍外还有硫磺、红磷、炭黑、石蜡.
(4)白磷通常保存在水中,而不放置在空气中的原因是白磷不溶于水,密度比水大,着火点低,在空气中放置易发生自燃.
(5)白磷与红磷性质不同的主要原因是白磷与红磷的分子结构不同.
19世纪50年代,白磷火柴在欧洲普遍流行.19世纪末,人们发现利用白磷做火柴的工人,易患一种磷毒性颌骨坏死的疾病,至此白磷的毒性受到关注.各国也在不同时期宣布禁止生产和销售白磷火柴,于是火柴上的白磷渐渐被红磷取代.现代火柴头主要成分是氯酸钾和硫磺,火柴盒侧面的磷皮则使用了红磷,辅料包括石蜡、二氧化锰、炭黑、黏合剂和稳定剂等.
纯净的白磷是无色透明的晶体,遇光会逐渐变黄,因而又叫黄磷.白磷剧毒,误食0.1g就能致死.白磷接触皮肤也会引起吸收中毒.白磷不溶于水,易溶于二硫化碳.经测定,白磷的分子式为P4.
白磷最特殊的性质就是能在潮湿的空气中发生缓慢氧化,反应产生的部分能量以光能的形式放出,故在暗处可看到白磷发光.当缓慢氧化积累的能量达到它的着火点(40℃)时便发生自燃,因此白磷通常储存在水中.
白磷和红磷虽然一字之差,但是它们的结构、着火点和毒性却有很大不同.白磷是剧毒、着火点低、四面体型分子,而红磷是无毒、着火点较高、链状分子
| 物质 性质 | 白磷 | 红磷 |
| 毒性 | 剧毒 | 无毒 |
| 着火点 | 40℃ | 240℃ |
分子结构 | 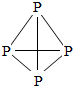 | 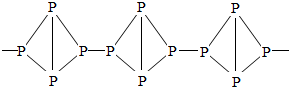 |
(1)白磷的物理性质无色固体(或不溶于水、易溶于二硫化碳等)(任写一条).
(2)白磷燃烧反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)现代火柴摩擦生火时燃烧的物质中,除木棍外还有硫磺、红磷、炭黑、石蜡.
(4)白磷通常保存在水中,而不放置在空气中的原因是白磷不溶于水,密度比水大,着火点低,在空气中放置易发生自燃.
(5)白磷与红磷性质不同的主要原因是白磷与红磷的分子结构不同.
4. 中国首座纯液态纯铅冷却剂实验回路日前在中科院调试成功,标志我国在“第四代核反应堆”
中国首座纯液态纯铅冷却剂实验回路日前在中科院调试成功,标志我国在“第四代核反应堆”
技术取得重大突破.右图为铅原子在元素周期表中的信息.则下列说法中正确的是( )
 中国首座纯液态纯铅冷却剂实验回路日前在中科院调试成功,标志我国在“第四代核反应堆”
中国首座纯液态纯铅冷却剂实验回路日前在中科院调试成功,标志我国在“第四代核反应堆”技术取得重大突破.右图为铅原子在元素周期表中的信息.则下列说法中正确的是( )
| A. | 铅原子的核电荷数为82 | B. | 铅原子的相对原子质量是207.2g | ||
| C. | 铅元素属于非金属元素 | D. | 铅原子的核外电子数为207 |
5.下列有关实验操作顺序中,“先”与“后”的说法正确的是( )
| A. | 制取气体时,先装入药品,后检查装置的气密性 | |
| B. | 用CO还原Fe2O3的实验结束后,先停止通入CO,后停止加热 | |
| C. | 稀释浓硫酸时,先把浓硫酸倒入烧杯中,后沿烧杯内壁缓慢注入水并搅拌 | |
| D. | 加热试管中的固体时,先预热试管,后用酒精灯外焰集中加热药品部位 |