题目内容
15.下列装置能达到对应实验目的是( )| A. | 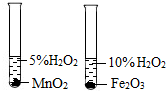 比较MnO2和Fe2O3的催化效果 | B. |  制取并收集CO2气体 | ||
| C. | 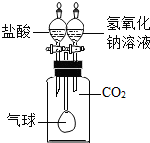 确认CO2和NaOH已发生反应 | D. | 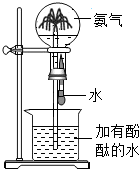 形成蓝色喷泉 |
分析 A、根据控制变量法的具体操作进行分析;
B、根据二氧化碳密度比空气大进行分析;
C、根据氢氧化钠和二氧化碳会生成碳酸钠,碳酸钠和盐酸会生成二氧化碳进行分析;
D、根据氨水显碱性,能使酚酞变红色进行分析.
解答 解:A、过氧化氢溶液的浓度不同,催化剂也不同,所以不能比较MnO2和Fe2O3的催化效果,故A错误;
B、二氧化碳密度比空气大,收集二氧化碳用向上排空气法,故B错误;
C、氢氧化钠和二氧化碳会生成碳酸钠,碳酸钠和盐酸会生成二氧化碳,通过气球的变化,判断确认CO2和NaOH已发生反应,故C正确;
D、氨水显碱性,能使酚酞变红色,会形成红色喷泉,故D错误.
故选:C.
点评 本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,完成此题,可以依据已有的知识进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.为了让天更蓝、地更绿、水更淸,下列建议不可行的是( )
| A. | 严禁随意焚烧秸秆,以减少PM2.5的排放 | |
| B. | 大力开发和使用风能、太阳能,减少使用化石燃料 | |
| C. | 禁止使用化肥农药,以防止水体污染 | |
| D. | 分类回收垃圾.以促进资源再生和利用 |
3.物质的性质决定用途,下列有关说法不正确的是( )
| A. | 洗洁精具有乳化功能,用于去除油污 | |
| B. | 用碳素墨水写文字档案,便于长期保存 | |
| C. | 石墨的导电性比铜差,故可用作半导体 | |
| D. | 钨丝的熔点高,可用于白炽灯的灯丝 |
10.有一含CaCO3与CaO的混合物,取该混合物16g,进行充分高温煅烧后,将剩余固体投入200g溶质质量分数为7.3%的稀盐酸中,恰好完全反应,则原混合物中钙元素的质量分数为( )
| A. | 30% | B. | 40% | C. | 50% | D. | 60% |
20.实验室有一瓶长期暴露有空气中的氢氧化钠样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只有含Na2CO3;
猜想Ⅱ:部分变质,该样品含有NaOH和Na2CO3.
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
【反思小结】固体氢氧化钠暴露在空气中,容易吸收水分而使表面潮湿并逐渐溶解,这种现象叫做①潮解;同时吸收空气中的二氧化碳而变质,生成碳酸钠,因此,氢氧化钠固体要②密封保存.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只有含Na2CO3;
猜想Ⅱ:部分变质,该样品含有NaOH和Na2CO3.
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入①过量的氯化钙溶液; | 白色沉淀产生 | 该反应的化学方程式为 ②Na2CO3+CaCl2═CaCO3↓+2NaCl |
| (2)将上述反应反的混合液过滤,取滤液加入①酚酞试液; | ②溶液变成红色 | 证明猜想Ⅱ成立. |
7.实验室加热高锰酸钾制氧气,可直接采用的发生装置是( )
| A. | 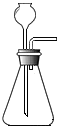 | B. |  | C. | 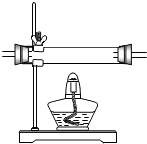 | D. | 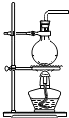 |
4.下列说法正确的是( )
| A. | 水果、米饭中富含蛋白质 | B. | 金属矿物资源可再生 | ||
| C. | 塑料容器都适合储存食物 | D. | 碳酸钙能用作补钙剂 |
5.下列食物中富含蛋白质的是( )
| A. | 奶油 | B. | 牛肉 | C. | 西红柿 | D. | 馒头 |
 金属活动性顺序在生产和科学研究中有重要应用.请回答下列问题:
金属活动性顺序在生产和科学研究中有重要应用.请回答下列问题: