题目内容
下列现象或事实,可用金属活动性作出合理解释的是
①黄铜(铜锌合金)外观与黄金相似,但可将两者放入稀盐酸中加以区别 ;
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强;
③用硫酸铜、石灰水配制农药波尔多液时,不能用铁制容器;
④铜的导电性比铁强
A.②④ B.①③ C.②③ D.①②③
B
【解析】①在金属活动性顺序表中,锌排在氢的前面,把黄铜放入盐酸中能产生气泡,黄金无现象,所以可以区分黄铜和黄金;②金属铝与空气中的氧气反应,生成致密的氧化物薄膜,使铝不被腐蚀,耐腐蚀性增强;③在金属活动性顺序表中,铁在铜的前面,铁能与硫酸铜反应,降低药效,所以不能用铁制容器配制波尔多液;④铜的导电性仅次于银,比铁强;故选B.
试题分析:根据铜、锌和金的金属活动性可知放入盐酸中黄铜表面有气泡产生分析;根据金属铝与氧气反应生成致密的氧化铝薄膜,可以隔绝空气,使铝的抗腐蚀性能增强分析;根据铁的活动性比铜强,能置换出硫酸铜中的铜分析;根据铜和铁的导电性强弱分析.
考点:金属的活动性顺序;金属的物理性质和用途;纯金属与合金的区别

(5分)在“质量守恒定律”的课堂教学中,甲、乙两组同学进行了“化学反应中,反应物与生成物的质量关系”的实验探究。实验装置和选用药品如图所示:
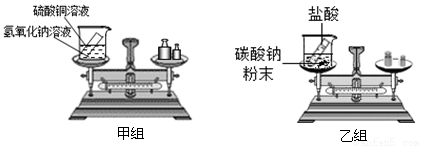
(提示:CuSO4+2NaOH==Na2SO4+Cu(OH)2↓;2HCl+Na2CO3==2NaCl+H2O+CO2↑)
(1)根据实验目的,两组同学应该测量的数据是_____________(填“只有反应前”“只有反应后”“反应前、后”之一)整个反应装罝(包括烧杯、试管和药品)的质量。
(2)实验过程中他们都进行了规范的操作、准确的称量和细致的观察:
现象 | 结论 | |
甲组 | 出现蓝色沉淀,天平平衡 | 质量守恒 |
乙组 | 出现大量气泡,天平不平衡 | 质量不守恒 |
乙组实验反应后天平不平衡,天平指针向 偏转(填“左”或“右”)。你认为结论正确的是 (填“甲组”或“乙组”),而导致另一组结论错误的原因是 。
(3)由质量守恒定律可知,化学反应前后,一定不变的是 。(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类

 意义的示意图是
意义的示意图是