题目内容
10.有14g赤铁矿的样品,经化验测定其中含铁元素质量为5.88g,则此赤铁矿中含三氧化二铁的质量分数为多少?分析 根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:有14g赤铁矿的样品,经化验测定其中含铁元素质量为5.88g,则此赤铁矿中含三氧化二铁的质量为5.88g÷($\frac{56×2}{56×2+16×3}×$100%)=8.82g.
此赤铁矿中含三氧化二铁的质量分数为$\frac{8.82g}{14g}×$100%=63%.
答:此赤铁矿中含三氧化二铁的质量分数为63%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20. 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )| A. | 用蒸发甲或乙的溶液中的水的方法可以得到甲或乙的晶体 | |
| B. | t2℃时,甲的溶解度是110g | |
| C. | tl℃时,甲、乙的两种溶液溶质的质量分数相等 | |
| D. | t2℃时,用210 g甲的饱和溶液加水可以配制成550g 20%的甲溶液 |
1.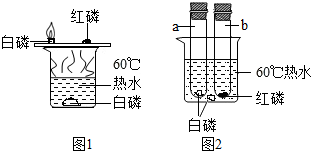 某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,发现白磷燃烧产生大量白烟,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).已知白磷的着火点是40℃,红磷的着火点是240℃,
某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,发现白磷燃烧产生大量白烟,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).已知白磷的着火点是40℃,红磷的着火点是240℃,
请回答:
(1)同学们对图1装置进行改进,按改进后的图2装置进行实验,改进后的装置优点是能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康,不足是白磷燃烧放热容易造成胶塞松动甚至弹出.
(2)请你帮助他们将下表补充完整.
(3)能说明空气是混合物的实验现象为:实验结束后,图2装置保持原样.待a试管冷却后,如果将试管口紧贴水面(室温下).并取下橡皮塞,观察到的现象是液体进入试管,但未装满试管.
 某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,发现白磷燃烧产生大量白烟,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).已知白磷的着火点是40℃,红磷的着火点是240℃,
某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,发现白磷燃烧产生大量白烟,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).已知白磷的着火点是40℃,红磷的着火点是240℃,请回答:
(1)同学们对图1装置进行改进,按改进后的图2装置进行实验,改进后的装置优点是能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康,不足是白磷燃烧放热容易造成胶塞松动甚至弹出.
(2)请你帮助他们将下表补充完整.
| 现象 | 解释 |
| a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. | b试管中红磷、热水中白磷都没有燃烧的原因是 ①温度未达到红磷的着火点; ②热水中的白磷没有与氧气(或空气)接触. |
18.实验证明M气体在空气中燃烧有水生成.仅据此结果,下列对M的成分推测正确的是( )
| A. | M是氢气 | B. | M是甲烷 | ||
| C. | M中一定含有氢元素 | D. | M中含有氢、氧两种元素 |
5.某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了以下制备(NH4)2SO4的工艺流程.在图流程中,沉淀池里物质发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4.
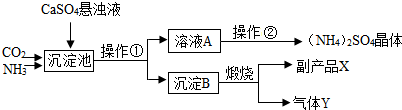
下列有关说法完全正确的是( )

下列有关说法完全正确的是( )
| A. | 沉淀B、副产品X分别是CaCO3和Ca(OH)2 | |
| B. | 操作①是过滤,实验室进行此操作时所用玻璃棒的作用是搅拌以加快速度 | |
| C. | 此流程中可循环使用的物质是CO2 | |
| D. | 得到的产品和副产品都是有用的物质,无废物产生 |
10.为预防非典型肺炎,公用场所可用过氧乙酸(C2H4O3)溶液来消毒.过氧乙酸属于下列物质类别中的( )
| A. | 混合物 | B. | 氧化物 | C. | 无机化合物 | D. | 有机化合物 |
 同学们在探究中和反应时发现有些反应有明显的现象,有些反应无明显的现象.
同学们在探究中和反应时发现有些反应有明显的现象,有些反应无明显的现象.