题目内容
4. 金属材料已得到越来越广泛的应用,请依据所学知识回答下列问题.
金属材料已得到越来越广泛的应用,请依据所学知识回答下列问题.(1)钢铁是最常用的金属材料.
①钢属于混合物(填“纯净物”或“混合物”);
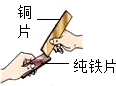
②将钢片和纯铁片相互刻画,纯铁片上留下划痕,说明钢比铁的硬度大.
③以赤铁矿(主要成分为氧化铁)为例,写出工业上高炉炼铁的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)铝制品比铁制品抗腐蚀性更好的原因是铝在空气中易被氧气氧化生成致密的氧化铝保护膜.
(3)向硝酸镁和硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,观察到滤液为无色,则该滤液中的溶质一定有硝酸锌和硝酸镁,滤渣中一定有铜.
分析 根据已有的金属的成分、合金与纯金属的硬度比较以及炼铁的原理进行分析解答,铝在空气中易被氧气氧化、根据金属活动性顺序的意义进行分析解答即可.
解答 解:(1)①钢是铁的合金,属于混合物,故填:混合物;
②将钢片和纯铁片相互刻画,纯铁片上留下划痕,说明钢比铁的硬度大,故填:钢比铁的硬度大.
③氧化铁和一氧化碳在高温下反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)铝制品比铁制品抗腐蚀性更好的原因是铝在空气中易被氧气氧化生成致密的氧化铝保护膜,起到了保护的作用,故填:铝在空气中易被氧气氧化生成致密的氧化铝保护膜.
(3)锌的活动性强于铜,比镁弱,故向硝酸镁和硝酸铜的混合溶液中加入一定量锌粉,锌能与硝酸铜反应生成硝酸锌和铜,锌与硝酸镁壶反应,充分反应后过滤,观察到滤液为无色,说明硝酸铜全部参加反应,则该滤液中的溶质一定为硝酸锌和硝酸镁,滤渣中一定有铜,故填:硝酸锌和硝酸镁,铜.
点评 本题考查的是金属的应用以及金属活动性顺序的应用,完成此题,可以依据已有的金属的性质以及金属活动性顺序的意义进行.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
15.由原子结构示意图为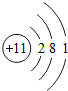 和
和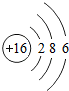 的两种元素组成的化合物,其化学式是( )
的两种元素组成的化合物,其化学式是( )
 和
和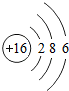 的两种元素组成的化合物,其化学式是( )
的两种元素组成的化合物,其化学式是( )| A. | Na2O | B. | NaCl | C. | Na2S | D. | CO2 |
12.将下列物质加入水中,所得溶液的pH可能为8的是( )
| A. | 生石灰 | B. | 柠檬酸 | C. | 白醋 | D. | 食盐 |
19.下列实验方案中,能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 分离氯化钙和氯化镁的混合溶液 | 加适量氢氧化钙溶液,充分反应后过滤 |
| B | 检验氢氧化钠溶液已部分变质 | 取少量溶液,滴加足量的氯化钡溶液,过滤,向滤液中滴加酚酞溶液 |
| C | 除去二氧化碳中混有的一氧化碳 | 将混合气体通过灼热的铜网 |
| D | 粗略测定空气中氧气的含量 | 用硫粉代替红磷在空气中燃烧 |
| A. | A | B. | B | C. | C | D. | D |
16.下列反应属于分解反应的是( )
| A. | H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑ | B. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | HC1+NaOH═NaCl+H2O |