题目内容
19. 如图中,①、④是紫色石蕊试液湿润的棉球,②、③是紫色石蕊试液染成紫色的干燥棉球.能说明CO2密度大于空气且能与水反应的现象是( )
如图中,①、④是紫色石蕊试液湿润的棉球,②、③是紫色石蕊试液染成紫色的干燥棉球.能说明CO2密度大于空气且能与水反应的现象是( )| A. | ①变红,③不变红 | B. | ④变红,③不变红 | ||
| C. | ①、④变红,②、③不变红 | D. | ④比①先变红,②、③不变红 |
分析 根据二氧化碳能和水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色解答.
解答 解:通入二氧化碳,用石蕊溶液染成紫色的干燥棉球②③都不变色,说明二氧化碳不能使石蕊变色,通二氧化碳,用紫色石蕊溶液润湿的棉球都变红,说明二氧化碳和水发生了化学反应.并且④比①先变红,说明二氧化碳的密度比空气的大.
故选:D
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.比较类推是学习中常用的思维方法,以下类推结果中,正确的是( )
| A. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 碱的水溶液显碱性,所以碱性溶液一定是碱溶液 | |
| C. | 溶液具有均一性和稳定性,所以均一的,稳定的混合物一定是溶液 | |
| D. | 活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属 |
6.按酸、碱、氧化物的顺序排列的一组物质是( )
| A. | CuO、H2SO4、Na2CO3 | B. | H2O、Ca(OH)2、Na2SO4 | ||
| C. | H2SO4、NaOH、Fe2O3 | D. | NaOH、H2CO3、CO2 |

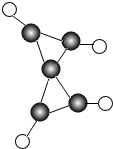 通过化学的学习,小明同学感悟到学习化学开拓了思维,增长了智慧.
通过化学的学习,小明同学感悟到学习化学开拓了思维,增长了智慧. ”代表碳原子,“
”代表碳原子,“ ”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O.
”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O.