题目内容
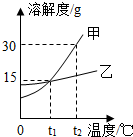 图为甲乙两物质的溶解度曲线,下列说法正确的是( )
图为甲乙两物质的溶解度曲线,下列说法正确的是( )| A、甲的溶解度大于乙的溶解度 |
| B、t1℃时,甲、乙两物质的溶解度均为15g |
| C、t2℃时,可以配制溶质质量分数为30%的甲溶液 |
| D、升高温度可使接近饱和的甲溶液转化为饱和溶液 |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、比较物质的溶解度大小须确定温度;
B、根据溶解度曲线交点的意义解答;
C、根据在t2℃时甲的溶解度计算分析;
D、根据甲的溶解度随温度变化的情况分析.
B、根据溶解度曲线交点的意义解答;
C、根据在t2℃时甲的溶解度计算分析;
D、根据甲的溶解度随温度变化的情况分析.
解答:解:A、比较物质的溶解度大小须确定温度,故错误;
B、由甲、乙的溶解度曲线可知,在t1℃时,甲、乙两物质的溶解度曲线交予一点,在t1℃时,甲、乙两物质的溶解度均为15g,故正确;
C、由甲的溶解度曲线可知,t2℃时甲的溶解度是30g,由饱和时质量分数的计算式
×100%可知,不能配制溶质质量分数为30%的甲溶液.故错误.
D、由甲的溶解度曲线可知,甲的溶解度随温度的升高而增大,升高温度不能使接近饱和的甲溶液转化为饱和溶,故错误.
故选:B.
B、由甲、乙的溶解度曲线可知,在t1℃时,甲、乙两物质的溶解度曲线交予一点,在t1℃时,甲、乙两物质的溶解度均为15g,故正确;
C、由甲的溶解度曲线可知,t2℃时甲的溶解度是30g,由饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
D、由甲的溶解度曲线可知,甲的溶解度随温度的升高而增大,升高温度不能使接近饱和的甲溶液转化为饱和溶,故错误.
故选:B.
点评:明确溶解度概念的含义,并能据溶解度曲线、饱和溶液中溶质的质量分数计算方法分析解答.

练习册系列答案
相关题目
下列物质中,属于纯净物的是( )
| A、金刚石 | B、空气 | C、海水 | D、碘酒 |
硅酸钠(Na2SiO3)可用作粘合剂和防火材料.硅酸钠中硅元素的化合价为( )
| A、+l | B、+2 | C、+3 | D、+4 |
恒温蒸发M溶液经如下变化:蒸发10g水,无固体析出,得N溶液;把N溶液蒸发10g水,析出3g固体,过滤得Z溶液.下列结论正确的是( )
| A、N溶液一定不饱和 |
| B、该溶质的溶解度为30g |
| C、N溶液溶质质量分数一定小于Z溶液溶质的质量分数 |
| D、若将Z溶液再蒸发掉10g水析出固体的质量可能大于3g |
造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
| A、分子很小 |
| B、分子在不断运动 |
| C、分子之间有间隔 |
| D、分子间有相互作用 |
在①Cu、Mg、C、Hg②CO2、CuO、P2O5、H20③液氧、糖水、石灰水、空气三组物质中,各有一种物质在分类上与组内其他物质不相同,这三种物质分别是( )
| A、Cu、P2O5、糖水 |
| B、Hg、CO、石灰水 |
| C、C、CuO、液氧 |
| D、Mg、H2O、空气 |
下列实验现象描述错误的是( )
| A、红磷在空气中燃烧,产生大量白色烟雾 |
| B、将二氧化碳通入紫色石蕊溶液中,溶液变红色 |
| C、红亮的铜丝在酒精灯火焰上灼烧,铜丝表面变黑 |
| D、氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 |