题目内容
如图是初中化学实验室中常见的几种仪器,请按要求回答下列问题.

(1)图中仪器C的名称是 ;仪器F的名称是 .
(2)写出实验室用氯酸钾和二氧化锰制取氧气的化学方程式 ,用该药品制取氧气并用排水法收集氧气需要用到的上面仪器有 (填序号)
(3)写出实验室制取二氧化碳的化学方程式 ,证明二氧化碳气体收集满的方法是将燃着的木条放 ,木条熄灭.

(1)图中仪器C的名称是
(2)写出实验室用氯酸钾和二氧化锰制取氧气的化学方程式
(3)写出实验室制取二氧化碳的化学方程式
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
用该药品制取氧气并用排水法收集氧气需要用到的上面仪器有试管、集气瓶、带导管的单孔橡皮塞、水槽和酒精灯;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳不能燃烧,不支持燃烧.
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
用该药品制取氧气并用排水法收集氧气需要用到的上面仪器有试管、集气瓶、带导管的单孔橡皮塞、水槽和酒精灯;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳不能燃烧,不支持燃烧.
解答:解:(1)图中仪器C的名称是烧杯,常用于配制溶液等;仪器F的名称是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品.
故填:烧杯;长颈漏斗.
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为:2KClO3
2KCl+3O2↑; 用该药品制取氧气并用排水法收集氧气需要用到的上面仪器有试管D、集气瓶E、带导管的单孔橡皮塞I、水槽J和酒精灯K.
故填:2KClO3
2KCl+3O2↑;DEIJK.
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
证明二氧化碳气体收集满的方法是将燃着的木条放在集气瓶口,木条熄灭.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;在集气瓶口.
故填:烧杯;长颈漏斗.
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为:2KClO3
| ||
| △ |
故填:2KClO3
| ||
| △ |
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
证明二氧化碳气体收集满的方法是将燃着的木条放在集气瓶口,木条熄灭.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;在集气瓶口.
点评:本题考查仪器的用途、装置的选择、化学方程式的书写、实验基本操作等方面的知识,只有综合掌握教材内容才能正确的做出解答.

练习册系列答案
相关题目
下列变化中,属于化学变化的是( )
| A、蜡烛燃烧 | B、酒精挥发 |
| C、瓷碗破碎 | D、水结成冰 |
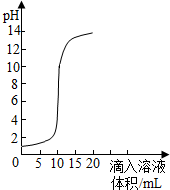 (1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成