题目内容
20g质量分数为20%的NaOH溶液能恰好和30g某稀盐酸完全中和,求:
(1)盐酸中溶质的质量分数?
(2)反应后的溶液中溶质的质量分数.
(1)盐酸中溶质的质量分数?
(2)反应后的溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据氢氧化钠溶液质量、质量分数可以计算盐酸中氯化氢的质量和反应生成氯化钠的质量,进一步可以计算盐酸中溶质的质量分数、反应后的溶液中溶质的质量分数.
解答:解:(1)设盐酸中氯化氢的质量为x,反应生成氯化钠的质量为y,
NaOH+HCl═NaCl+H2O,
40 36.5 58.5
20g×20% x y
=
=
,
x=3.65g,y=5.85g,
盐酸中溶质的质量分数为:
×100%=12.1%,
答:盐酸中溶质的质量分数为12.1%.
(2)反应后的溶液中溶质的质量分数为:
×100%=11.7%,
答:反应后的溶液中溶质的质量分数为11.7%.
NaOH+HCl═NaCl+H2O,
40 36.5 58.5
20g×20% x y
| 40 |
| 20g×20% |
| 36.5 |
| x |
| 58.5 |
| y |
x=3.65g,y=5.85g,
盐酸中溶质的质量分数为:
| 3.65g |
| 30g |
答:盐酸中溶质的质量分数为12.1%.
(2)反应后的溶液中溶质的质量分数为:
| 5.85g |
| 20g+30g |
答:反应后的溶液中溶质的质量分数为11.7%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
物质的性质决定其用途.下列对应关系错误的是( )
| A、氢氧化钙可用来改良酸性土壤----氢氧化钙溶液呈碱性 |
| B、浓硫酸常用作气体干燥剂----浓硫酸具有吸水性 |
| C、氢氧化钠用于治疗胃酸过多----氢氧化钠能与酸反应 |
| D、氧化钙可做食品干燥剂----氧化钙能与水反应 |
下列各组物质中,按混合物、化合物、单质顺序排列的是( )
| A、冰水共存物、干冰、氮气 |
| B、洁净的空气、二氧化硫、液态氧 |
| C、石油、煤、天然气 |
| D、氯酸钾、酒精、水银 |
一位同学要称量2.5g药品用于实验,在称量过程中发现指针向右偏转,这时他应该( )
| A、减少药品 |
| B、添加药品 |
| C、调节天平平衡螺母 |
| D、移动游码 |
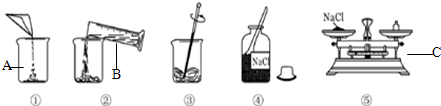
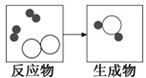 如图是某化学反应的微观粒子示意图.
如图是某化学反应的微观粒子示意图.  B.两个
B.两个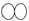 C.一个
C.一个  D.两个
D.两个