题目内容
2.为测定某Cu-Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物的质量为49.8克.(1)生成氢气的质量为0.1g;
(2)计算原合金中铜的质量分数.
分析 根据黄铜的成分铜和锌的性质可知,加入稀硫酸时,只有锌与硫酸反应生成了硫酸锌和氢气;根据质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,据此根据反应的化学方程式列式计算出参加反应锌的质量,进而计算出铜的质量和铜的质量分数.
解答 解:(1)根据质量守恒定律,产生氢气的质量为:10g+40g-49.9g=0.1g;
(2)设黄铜样品中锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.1g
$\frac{65}{2}=\frac{x}{0.1g}$
x=3.25g
黄铜样品中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%
答案:(1)0.1g;(2)黄铜样品中铜的质量分数为67.5%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
12.下面是李好同学用连线的方式对某主题知识进行归纳的情况,其中有错误的一组是( )
| A. | 性质与用途:氢气燃烧产物为水--最理想燃料 熟石灰呈碱性--改良酸性土壤 活性炭有吸附性--做净水剂 | |
| B. | 元素与人体健康:人体缺氟--易生龋牙 人体缺锌--影响人体发育 人体缺碘--甲状腺肿大 | |
| C. | 生活常识:取暖防中毒--煤炉上放一壶水 防菜刀生锈--喷水后悬挂起来 海鲜品保鲜--甲醛水溶液浸泡 | |
| D. | 环保与物质的利用:减少水污染--合理使用农药、化肥 减少汽车尾气污染--使用乙醇汽油 减少白色污染--使用可降解的塑料 |
10.化学实验中处处表现了颜色变化美,下列化学实验中的颜色变化不符合实验事实的是( )
| A. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| B. | 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色 | |
| C. | 在水中加入少量高锰酸钾,液体由无色变成紫红色 | |
| D. | 用一氧化碳还原氧化铁时,固体由红色变成黑色 |
14.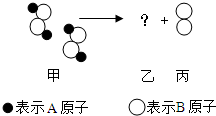 如图所示,每二个甲分子反应后生成二个乙分子和一个丙分子,已知甲、乙、丙分别为不同的纯净物.则从图中获得的信息中,不正确的是( )
如图所示,每二个甲分子反应后生成二个乙分子和一个丙分子,已知甲、乙、丙分别为不同的纯净物.则从图中获得的信息中,不正确的是( )
 如图所示,每二个甲分子反应后生成二个乙分子和一个丙分子,已知甲、乙、丙分别为不同的纯净物.则从图中获得的信息中,不正确的是( )
如图所示,每二个甲分子反应后生成二个乙分子和一个丙分子,已知甲、乙、丙分别为不同的纯净物.则从图中获得的信息中,不正确的是( )| A. | 在该反应中,分子发生了改变 | |
| B. | 该化学反应的类型为分解反应 | |
| C. | 该反应生成的乙物质属于化合物 | |
| D. | 一个乙分子中含1个A原子和1个B原 子 |
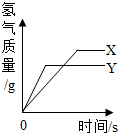 将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答:
将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答: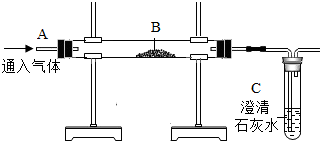 用如图装置完成以下试验:
用如图装置完成以下试验: