题目内容
5.2016年1月29日《科技日报》报道:科学家首次将从空气捕获的二氧化碳用氢气将其转化为甲醇,同时有水生成.该研究即可除去大气中的温室气体二氧化碳,生成的甲醇还能作为汽油的替代燃料.二氧化碳转化成甲醇的过程中,一个关键的因素是找到合适的均相催化剂.此次研究人员开发出在高温下不会分解的金属钌催化剂,稳定性好,可重复使用.(1)二氧化碳转化成甲醇的微观示意图,如图所示.
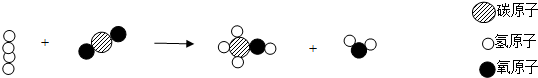
①此反应中的化合物有3种,其中属于有机化合物的是甲醇.
②请写出这一反应的化学方程式CO2+3H2$\frac{\underline{\;催化剂\;}}{\;}$CH3OH+H2O.
(2)请写出甲醇完全燃烧的化学方程式2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O.
分析 由两种或两种以上元素组成的纯净物属于化合物;
含有碳元素的化合物属于有机化合物,其中二氧化碳、一氧化碳、碳酸盐等除外;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)①此反应中的化合物有二氧化碳、甲醇和水等3种,其中属于有机化合物的是甲醇,二氧化碳虽然是含有碳元素的化合物,但是不属于有机化合物.
故填:3;甲醇.
②二氧化碳和氢气在催化剂作用下反应生成甲醇和水的化学方程式为:CO2+3H2$\frac{\underline{\;催化剂\;}}{\;}$CH3OH+H2O.
故填:CO2+3H2$\frac{\underline{\;催化剂\;}}{\;}$CH3OH+H2O.
(2)甲醇完全燃烧生成水和二氧化碳,反应的化学方程式为:2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O.
故填:2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
15.2015年2月28日,柴静关于环保的纪录片《穹顶之下》在短时间内引起广泛关注.近年来雾霾天气一度笼罩我国中东部大部分地区,多地PM2.5指数直逼最大值.下列行为不利于雾霾天气治理的是( )
| A. | 以步代车 | B. | 风力发电 | C. | 焚烧垃圾 | D. | 植树造林 |
13.对下列四种粒子的结构示意图的理解,错误的是( )
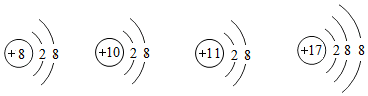
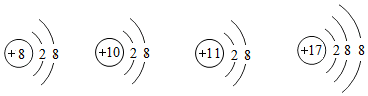
| A. | 它们都带电荷 | B. | 它们都具有相对稳定结构 | ||
| C. | 它们的核外电子排布不完全相同 | D. | 它们属于不同种元素 |
17.下列实验操作错误的是( )
| A. | 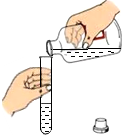 倾倒液体 | B. | 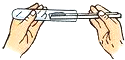 装入固体粉末 | C. | 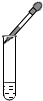 滴加液体 | D. | 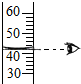 读取液体体积 |
15.甲同学对有关盐的知识进行了以下的整理.
(1)填写下表空格中的化学式:
反思:①根据以上盐中的金属元素的排列,可以得出是依据顺序归纳整理的.
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液一定(填“一定”或“不一定”)具有相似的化学性质,因为因为溶液中都解离出共同的Cl-.
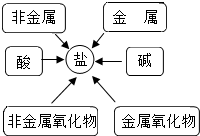
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成如图.
验证:请写出下列有盐生成的部分化学方程式:
①用稀硫酸除铁锈:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
②盐酸和氢氧化钠反应:HCl+NaOH=NaCl+H2O;
③古代记载的湿法冶金技术有“曾青得铁则化为铜”:(“曾青”指硫酸铜溶液):Fe+CuSO4=Cu+FeSO4;属于置换反应.
(1)填写下表空格中的化学式:
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | FeCl2 | CuCl2 |
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液一定(填“一定”或“不一定”)具有相似的化学性质,因为因为溶液中都解离出共同的Cl-.
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成如图.
验证:请写出下列有盐生成的部分化学方程式:

①用稀硫酸除铁锈:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
②盐酸和氢氧化钠反应:HCl+NaOH=NaCl+H2O;
③古代记载的湿法冶金技术有“曾青得铁则化为铜”:(“曾青”指硫酸铜溶液):Fe+CuSO4=Cu+FeSO4;属于置换反应.


