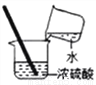
��Ŀ����
��a��b��c���ֽ����ֱ�Ͷ��ϡ�����AgNO3��Һ�У���������ʵ������
���� | a | b | c |
ϡ���� | a�ܽⲢ�������� | �����Ա仯 | �����Ա仯 |
AgNO3��Һ | a����������ɫ�������� | �����Ա仯 | c����������ɫ�������� |
��a��b��c���ֽ����Ļ����ǿ������˳����( )
A. a>b>c B. c>b>a C. b>a>c D. a>c>b
D ����������������Ϣ֪������ϡ���ᣬa�ܽⲢ�������ݣ�b��c�������Ա仯��˵��a��b,c���ã�����AgNO3��Һ��a����������ɫ����������b�����Ա仯,c����������ɫ����������˵��c��b���ã���a��b��c���ֽ����Ļ����ǿ������˳����a>c>b����ѡD�� �㾦�ý����˳�����Ӧ�â�������ǰ��Ľ���������ϡ��������ᷴӦ�û������������������Ľ������ܢ�����ǰ����������������...
��ϰ��ϵ�д�
�����Ŀ



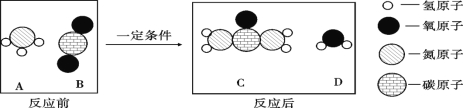
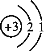 , д�����ϡ���ᷴӦ�Ļ�ѧ����ʽ ��
, д�����ϡ���ᷴӦ�Ļ�ѧ����ʽ �� B.
B. 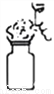 C.
C.  D.
D.