题目内容
2. 新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.(1)帕拉米韦由四种元素组成,其中氢、氮的原子个数比为7:1.
(2)帕拉米韦的相对分子质量是328
(3)帕拉米韦中氧元素的质量分数是19.5%(精确到0.1%).
(4)164g帕拉米韦中氮元素的质量是28 g.
(5)成人禽流感患者,每天应注射帕拉米韦6支.
分析 (1)根据化学式的意义进行分析判断.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(4)元素的质量=化合物的质量×化合物中该元素的质量分数;
(5)若每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,据此进行分析解答.
解答 解:(1)由帕拉米韦的化学式可知,它是由碳、氢、氧、氮四种元素的,其中氢、氮的原子个数比为28:4=7:1,故填:四;7:1.
(2)帕拉米韦的相对分子质量为12×15+1×28+14×4+16×4=328.故填:328;
(3)帕拉米韦中氧元素的质量分数=$\frac{16×4}{328}×100%$≈19.5%.故填:19.5%;
(4)164g帕拉米韦中氮元素的质量是$\frac{14×4}{328}×100%$=28g;故填:28;
(5)每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,则成人每日需注射量为75mg/次×2次=150mg,则每天应注射帕拉米韦注射液150mg÷25mg/支=6支.故填:6.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
12.集气瓶内充满某种气体,将带火星的木条伸入该气体,木条复燃,该气体一定是( )
| A. | 二氧化碳 | B. | 空气 | C. | 氧气 | D. | 氮气 |
17.如图所示的实验操作中正确的是( )
| A. | 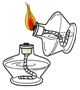 点燃酒精灯 | B. | 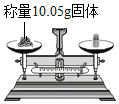 | C. | 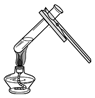 液体加热 | D. |  |
11.下列化学符号正确的是( )
| A. | 1个一氧化碳分子:Co | B. | 2个碳酸根离子:2CO32 | ||
| C. | 3个铁离子:3Fe2+ | D. | 4个氢原子:2H2 |
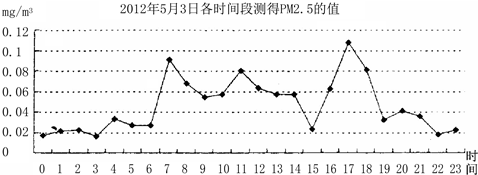
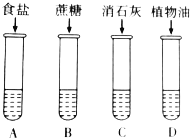 如图所示,用量简各量取5mL水加入A、B、C、D四支试管中,再分别加入食盐5g,蔗糖5g、消石灰(熟石灰)5g、植物油5滴,振荡片刻,静置,观察现象.
如图所示,用量简各量取5mL水加入A、B、C、D四支试管中,再分别加入食盐5g,蔗糖5g、消石灰(熟石灰)5g、植物油5滴,振荡片刻,静置,观察现象.