题目内容
4. “春蚕到死丝方尽,蜡炬成灰泪始干”,请回答下列问题.
“春蚕到死丝方尽,蜡炬成灰泪始干”,请回答下列问题.(1)这里“丝”的主要成分是蛋白质,用这种材料织成的布所具有的特点是A.
A.吸水性、透气性好 B.强度高、弹性好
C.舒适、不易褶皱 D.耐磨、耐腐蚀
(2)“蜡炬成灰”属于化学变化.石蜡是石油炼制的产品之一,除此之外还有许多不同的产品可以做燃料,汽车上使用乙醇汽油做燃料的好处是节约化石燃料,使用乙醇汽油可减少大气污染.
现代社会对能量的需求越来越大,太阳能热水器的能量转化为太阳能转化为热能.
(3)化石燃料的燃烧会导致环境污染,我省的冬季主要利用燃煤采暖,下列环境问题与燃煤有直接关系的有(多选)ABC.
A.酸雨 B.温室效应 C.PM2.5 D.臭氧空洞.
分析 (1)根据蚕丝是天然纤维,主要成分是蛋白质进行解答;
(2)根据“蜡炬成灰”是蜡烛燃烧以及太阳能热水器的能量转化为太阳能转化为热能进行解答;
(3)根据煤燃烧的产物回答本题.
解答 解:(1)蚕丝是天然纤维,主要成分是蛋白质,用这种材料织成的布所具有的特点是吸水性、透气性好;故填:蛋白质;A;
(2)“蜡炬成灰”是蜡烛燃烧,属于化学变化;汽车上使用乙醇汽油做燃料的好处是节约化石燃料,使用乙醇汽油可减少大气污染;太阳能热水器的能量转化为太阳能转化为热能;故填:化学;节约化石燃料,使用乙醇汽油可减少大气污染;太阳能转化为热能;
(3)将煤燃烧能生成二氧化碳、二氧化硫等物质,还能产生大量的灰尘,生成的二氧化碳能形成温室效应,生成的二氧化硫能形成酸雨,产生的大量灰尘增加了空气中的可吸入颗粒物;与破坏臭氧层无关,故选:ABC.
点评 本考点考查了材料和有关能源的问题,节约化石能源,合理的开发新能源是科学家们正在研究的新课题,有关能源问题也是近几年中考的热点之一,同学们要认真把握.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
14.2014年“世界水日”的宣传主题是“水与能源”.下列关于水的说法错误的是( )
| A. | 电解水时,能量由化学能转化为电能 | |
| B. | 可用肥皂水鉴别硬水和软水 | |
| C. | 利用太阳能使水分解是最理想的氢能来源 | |
| D. | 水通过三态变化实现天然循环,太阳为其提供能量 |
15.学校食堂提供的午餐食谱如下.请回答:
(1)走进食堂.能闻到香味,说明分子具有的性质是不断运动的.
(2)合理膳食.副食中,富含蛋白质的是清蒸鲈鱼.
(3)健康饮品.
①白开水容易解渴,促进新陈代谢,有调节体温、输送养分等功能.白开水是混合物(填“纯净物”或“混合物”).
②碳酸饮料中含有碳酸和柠檬酸等酸性物质,过量摄入会影响某元素的吸收,儿童缺少该元素可能导致佝偻病,该元素为钙.
③酸奶经过发酵,使奶中糖、蛋白质水解成为小的分子(如乳酸等)益于消化,乳酸的化学式为C3H6O3,依据化学式计算出相对分子质量为90,计算式为12×3+1×6+16×3.
(4)不使用一次性餐具也是一种健康的饮食习惯.
①竹木筷子、塑料水杯、不锈钢勺子所使用的材料中,属于有机合成高分子材料的是塑料水杯.
②普遍使用的陶瓷餐盘的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是+4,CaSiO3中硅元素和氧元素的质量比为7:12.
(5)厨房清洁.
①“管道通”可使堵塞的管道畅通无阻,其有效成分之一为氢氧化钠.在使用时禁止与皮肤接触,其原因是NaOH具有强烈的腐蚀性.
②利用厨房中食醋的可以溶解水壶中的水垢.
| 主食 | 馒头、米饭 |
| 副食 | 红烧牛肉、清蒸鲈鱼、凉拌黄瓜、清炒芹菜 |
| 饮品 | 白开水、酸奶 |
(2)合理膳食.副食中,富含蛋白质的是清蒸鲈鱼.
(3)健康饮品.
①白开水容易解渴,促进新陈代谢,有调节体温、输送养分等功能.白开水是混合物(填“纯净物”或“混合物”).
②碳酸饮料中含有碳酸和柠檬酸等酸性物质,过量摄入会影响某元素的吸收,儿童缺少该元素可能导致佝偻病,该元素为钙.
③酸奶经过发酵,使奶中糖、蛋白质水解成为小的分子(如乳酸等)益于消化,乳酸的化学式为C3H6O3,依据化学式计算出相对分子质量为90,计算式为12×3+1×6+16×3.
(4)不使用一次性餐具也是一种健康的饮食习惯.
①竹木筷子、塑料水杯、不锈钢勺子所使用的材料中,属于有机合成高分子材料的是塑料水杯.
②普遍使用的陶瓷餐盘的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是+4,CaSiO3中硅元素和氧元素的质量比为7:12.
(5)厨房清洁.
①“管道通”可使堵塞的管道畅通无阻,其有效成分之一为氢氧化钠.在使用时禁止与皮肤接触,其原因是NaOH具有强烈的腐蚀性.
②利用厨房中食醋的可以溶解水壶中的水垢.
19.下列不属于大气污染的是( )
| A. | 二氧化碳 | B. | 可吸入颗粒物 | C. | 二氧化硫 | D. | 一氧化碳 |
9.把pH=3的溶液与pH=6的溶液充分混合,所得溶液的pH值可能是( )
| A. | 2 | B. | 5 | C. | 9 | D. | 无法确定 |
2. 溶液在生命活动和生产、生活中都起到十分重要的作用.
溶液在生命活动和生产、生活中都起到十分重要的作用.
(1)将下面调味品加入水中,不能形成溶液的是DA.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为酒精.(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
①实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是e(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c<d(填“<”、“>”或“=”).
④取实验d所得溶液,若使其质量分数变为30%,在不改变温度的情况下,可以采取的操作是加入78.3克水.
(4)在不同温度时某物质A的溶解度如上表:根据表中信息,判断下列说法不正确的是D.
A.20℃时,A的溶解度为0.16g
B.40℃时,升高A的饱和溶液温度会析出溶质
C.60℃时,向100g水中加入0.20gA充分搅拌,固体不能完全溶解
D.A的溶解度随温度的升高而增大
(5)如图是一瓶开启的“XX牌”碳酸饮料的示意图,请回答:
开启时,大量的气泡从罐内冒出,说明随着压强的减小,气体的溶解度减小.
(6)实验室配制质量分数4%的氯化钠溶液50g,需要固体氯化钠的质量为2g,用量筒量取48mL水(水的密度1g/cm3).
(7)若用质量分数为8%的氯化钠溶液配制50g质量分数为4%的氯化钠溶液,要8%的氯化钠溶液的质量为25g.
 溶液在生命活动和生产、生活中都起到十分重要的作用.
溶液在生命活动和生产、生活中都起到十分重要的作用.(1)将下面调味品加入水中,不能形成溶液的是DA.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为酒精.(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d | e |
| 加入KNO3固体的质量 | 40 | 45 | 50 | 55 | 60 |
| 所得溶液质量 | 90 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c<d(填“<”、“>”或“=”).
④取实验d所得溶液,若使其质量分数变为30%,在不改变温度的情况下,可以采取的操作是加入78.3克水.
| 温度/ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 0.18 | 0.16 | 0.14 | 0.11 | 0.09 |
A.20℃时,A的溶解度为0.16g
B.40℃时,升高A的饱和溶液温度会析出溶质
C.60℃时,向100g水中加入0.20gA充分搅拌,固体不能完全溶解
D.A的溶解度随温度的升高而增大
(5)如图是一瓶开启的“XX牌”碳酸饮料的示意图,请回答:
开启时,大量的气泡从罐内冒出,说明随着压强的减小,气体的溶解度减小.
(6)实验室配制质量分数4%的氯化钠溶液50g,需要固体氯化钠的质量为2g,用量筒量取48mL水(水的密度1g/cm3).
(7)若用质量分数为8%的氯化钠溶液配制50g质量分数为4%的氯化钠溶液,要8%的氯化钠溶液的质量为25g.
3.取一滤纸条,等间距滴加紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象.下列有关说法不正确的是( )

| A. | 氨水的pH大于7 | |
| B. | 酸、碱能使酸碱指示剂显示不同颜色 | |
| C. | 所有分子的运动速率都相等 | |
| D. | 氨分子和氯化氢分子在不断运动 |
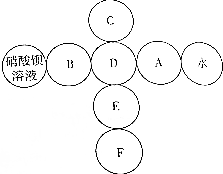 复习时,小东用水、硝酸钡溶液等物质玩起了化学游戏一“连连看”(如下图所示),其中A、B、C、D、E、F分别是氢氧化钡溶液、硝酸银溶液、硫酸钠溶液、碳酸钠溶液、氧化钙、稀盐酸中的一种.游戏规则要求相连接的两物质之间能发生化学反应,且D与E物质反应时无明显现象.请你和小东一起完成游戏,并回答下列问题:
复习时,小东用水、硝酸钡溶液等物质玩起了化学游戏一“连连看”(如下图所示),其中A、B、C、D、E、F分别是氢氧化钡溶液、硝酸银溶液、硫酸钠溶液、碳酸钠溶液、氧化钙、稀盐酸中的一种.游戏规则要求相连接的两物质之间能发生化学反应,且D与E物质反应时无明显现象.请你和小东一起完成游戏,并回答下列问题: