题目内容
19. 过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解水和氧气,而导致双氧水浓度降低.实验室现有一瓶未曾使用过的、久置的双氧水,如图为瓶上的标签.经过测定后发现瓶内的双氧水实际质量为904克.
过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解水和氧气,而导致双氧水浓度降低.实验室现有一瓶未曾使用过的、久置的双氧水,如图为瓶上的标签.经过测定后发现瓶内的双氧水实际质量为904克.(1)计算这瓶双氧水中过氧化氢的质量分数.
(2)若用这瓶双氧水配置H2O2的质量为数为3%的医用双氧水1500g,需要这种双氧水的质量是多少?
分析 过氧化氢在二氧化锰的催化作用下生成水和氧气,根据质量守恒定律,减少的质量即为生成氧气的质量,由反应的化学方程式列式计算出参加反应的过氧化氢的质量,据此结合根据溶液稀释前后溶质的质量不变,进行分析解答.
解答 解:(1)由质量守恒定律,生成氧气的质量为1000g-904g=96g.
设参加反应的过氧化氢的质量为x
2H2O2═2H2O+O2↑
68 32
x 96g
$\frac{68}{32}=\frac{x}{96g}$ x=204g.
这瓶双氧水中过氧化氢的质量分数为$\frac{1000g×30%-204g}{904g}$×100%≈10.6%.
(2)设需要这种双氧水的质量为x,根据溶液稀释前后溶质的质量不变,
则1500g×3%=x×10.6% x≈424.5g.
答:(1)这瓶双氧水中过氧化氢的质量分数为10.6%;
(2)需要这种双氧水的质量是424.5g.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算、溶液稀释前后溶质的质量不变即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
9.逻辑推理是化学学习中常用的思维方法,下面推理中正确的是( )
| A. | 酸中都有氢元素,所以含有氢元素的化合物一定是酸 | |
| B. | 酸性溶液能使石蕊试液变红色,所以能使石蕊溶液变红的溶液一定是酸性溶液 | |
| C. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 | |
| D. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
10.在点燃条件下,甲、乙反应的微观示意图如下.下列说法正确的是( )
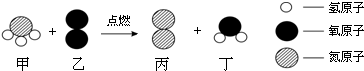

| A. | 该反应属于化合反应 | B. | 一定条件下,丁可转化为乙 | ||
| C. | 反应中甲、乙的分子数比为1:1 | D. | 反应前后元素的化合价都改变了 |
4.下列有关说法正确的是( )
| A. | 家里电器着火,立刻用水扑灭 | |
| B. | 楼层高的室内着火,立刻打开门窗 | |
| C. | 室内着火,火势较大,应该卧着向外爬出 | |
| D. | 家里油锅着火,立刻用水浇灭 |
12.我国在1993年成功制取了一种由相对原子质量为18,核电荷数为8的氧原子构成的双原子分子的气体,下列说法正确的是( )
| A. | 这种氧原子的核外电子数为10 | |
| B. | 这种氧原子的核内质子数为10 | |
| C. | 这种气体的相对分子质量为32 | |
| D. | 这种氧原子和氢原子构成水分子的相对分子质量为20 |
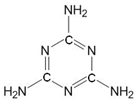 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示). 三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.由三元素组成,它的化学式为C3H6N6.(化学式书写按碳、氢、氧、其他元素的顺序写)
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示). 三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.由三元素组成,它的化学式为C3H6N6.(化学式书写按碳、氢、氧、其他元素的顺序写)