题目内容
18.某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的文字表达式是氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;Ⅱ中x的值应为1.0 g.
②乙探究了影响双氧水分解速度的某种因素.实验数据记录如表
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生 | O2体积 |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
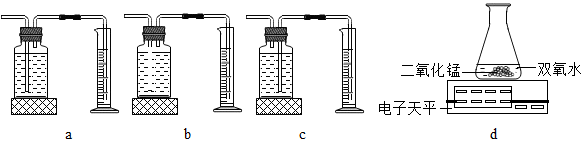
本实验中,为准确测得相同时间内产生O2体积,应在b(填编号)开始收集.
a.导管口有连续均匀气泡冒出时 b.导管口刚有气泡冒出时
实验结论:在相同条件下,双氧水浓度越大,双氧水分解得越快.丙用如图d装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.
分析 氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;控制变量法只能控制一个变量,因此X是1.0;本实验中,测量O2体积的装置是C,因为氧气密度比水的密度小,必须从短管进入,才能把水排出来;由表格信息可知:在相同条件下,双氧水浓度越大,双氧水分解得快;如果用双氧水制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.
解答 解:①氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,;控制变量法只能控制一个变量,因此X是1.0;故答案为:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;1.0;
②本实验中,测量O2体积的装置是c,因为氧气密度比水的密度小,必须从短管进入,才能把水排出来;故答案为:c;
由表格信息可知:在相同条件下,双氧水浓度越大,双氧水分解得快;如果用双氧水制氧气就不需要加热,而要完成本实验,必须用到F,才能测量出水的体积,进而测得生成氧气的体积,所以答案应为AF;故答案为:AF;双氧水的浓度越大;
本实验中,为准确测得相同时间内产生O2体积,应在导管口刚有气泡冒出时开始收集.故填:b;
在相同条件下,过氧化氢的浓度越大,双氧水分解得越快;乙用d图装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.
故填:双氧水浓度越大;相同时间天平读数差值大小(其它合理也可).
点评 本题通过实验探究了二氧化锰在过氧化氢制氧气中的催化作用,侧重实验能力和分析能力的考查.

练习册系列答案
相关题目
9.下列现象的微观解释中,不正确的是( )
| A. | 氢气和液氢都可做燃料(相同物质的分子,其化学性质相同) | |
| B. | 用警犬搜救地震中被埋人员(分子在不断运动) | |
| C. | 水烧开后易把壶盖冲起(温度升高,分子变大) | |
| D. | 用水银温度计测量体温(温度升高,原子间间隔变大) |
10.下列变化属于物理变化的是( )
| A. | 纸张燃烧 | B. | 葡萄酿成酒 | C. | 米饭变馊 | D. | 西瓜榨汁 |
5.下列属于节约用水标志的是( )
| A. |  | B. |  | C. |  | D. |  |
 鳔是鱼体密度的调节器官.已知某种鱼的鱼鳔内氧气的体积分数约占25%,其余主要是二氧化碳和氮气.两组同学对这种鱼鳔内的气体进行探究.
鳔是鱼体密度的调节器官.已知某种鱼的鱼鳔内氧气的体积分数约占25%,其余主要是二氧化碳和氮气.两组同学对这种鱼鳔内的气体进行探究.