题目内容
3.根据题如图所示装置,结合所学知识回答下列问题.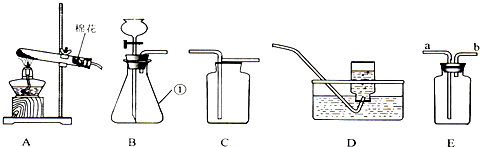
(1)E装置中充满水时,也可以作为氧气的收集装置,则氧气应从b端通入(填“a”或“b”);
(2)实验室用B装置制取氧气,写出反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)装置B中使用分液漏斗的优点是控制液体的滴加速度,进而控制反应速度;
(4)实验室用D装置收集氧气,当有大气泡从集气瓶口气泡冒出时说明已收集满.
分析 (1)根据氧气不易溶于水分析进气口;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)根据分液漏斗的特点解答;
(4)根据排水法收集氧气解答.
解答 解:(1)因为氧气不易溶于水,因此氧气从短管进入,把水从长管排出进行收集;
(2)实验室用B装置制取氧气不需要加热,应该是利用过氧化氢溶液和二氧化锰制取氧气,该反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)分液漏斗能够控制液体药品的用量,从而可以控制反应的速率,同时可以节约液体药品;
(4)排水法收集氧气,当有大气泡从集气瓶口气泡冒出时,说明已收集满.
故答案为:(1)b;(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)控制液体的滴加速度,进而控制反应速度;
(4)有大气泡从集气瓶口气泡冒出
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
13.下列物质的转变,不能由一步反应实现的是( )
| A. | CuO─→Cu(OH)2 | B. | Ca(OH)2─→NaOH | C. | CO2─→CaCO3 | D. | MgCl2─→Mg(NO3)2 |
11.酸和碱的知识是九年级化学学习的重要知识.请回答下列有关问题:
(1)下列说法中不正确的是BD.(填字母代号)
A.酸和碱都含有氢元素 B.生成盐和水的反应一定是中和反应
C.多数酸和碱有腐蚀性 D.酸和碱能与所有的盐发生复分解反应
(2)为探究酸、碱的化学性质,某小组做了如图所示实验.
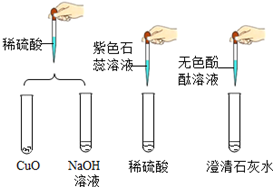
I、实验后某试管中为红色溶液,向其中加入一定量的某溶液后,红色消失变为无色,该反应的化学方程式为2HCl+Ca(OH)2═CaCl2+2H2O.
II、实验结束后,将得到的蓝色溶液和无色溶液倒入同一个干净的烧杯中,可观察到有蓝色沉淀生成,解释其原因?2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(3)某敞口放置的氢氧化钠溶液已变质,用方程式表示其变质的原因2NaOH+CO2═Na2CO3+H2O.
为证明该瓶氢氧化钠溶液未完全变质,设计了以下实验,请将表格填写完整.
(1)下列说法中不正确的是BD.(填字母代号)
A.酸和碱都含有氢元素 B.生成盐和水的反应一定是中和反应
C.多数酸和碱有腐蚀性 D.酸和碱能与所有的盐发生复分解反应
(2)为探究酸、碱的化学性质,某小组做了如图所示实验.

I、实验后某试管中为红色溶液,向其中加入一定量的某溶液后,红色消失变为无色,该反应的化学方程式为2HCl+Ca(OH)2═CaCl2+2H2O.
II、实验结束后,将得到的蓝色溶液和无色溶液倒入同一个干净的烧杯中,可观察到有蓝色沉淀生成,解释其原因?2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(3)某敞口放置的氢氧化钠溶液已变质,用方程式表示其变质的原因2NaOH+CO2═Na2CO3+H2O.
为证明该瓶氢氧化钠溶液未完全变质,设计了以下实验,请将表格填写完整.
| 实验操作 | 现象 | 结论 |
| 取少量该样品,滴入足量的 CaCl2溶液,充分反应后过滤. | 有白色沉淀生成 | 有关反应的化学方程式: CaCl2+Na2CO3═CaCO3↓+2NaCl |
| 在滤液中,滴入几滴 无色酚酞试液 | 溶液变红 | 样品未完全变质,仍含有氢氧化钠. |
12.写出下列溶液中的溶质、溶剂或溶液的名称:
| 溶液 | 盐酸 | 澄清石灰水 | 碘酒 | ||
| 溶质 | 氯化钠 | 氢氧化钠 | |||
| 溶剂 | 水 | 水 |
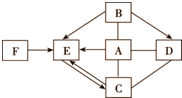 A~F为初中化学常见物质,这六种物质间存在右图所示的关系(“→”表示转化关系,“-”表示反应关系).其中A、B两溶液发生中和反应可得到厨房内常用的一种调味品和物质E;C在农业上可用来配制波尔多液,且C和D反应可制得B;A和D反应与A和小苏打反应得到的产物完全相同.
A~F为初中化学常见物质,这六种物质间存在右图所示的关系(“→”表示转化关系,“-”表示反应关系).其中A、B两溶液发生中和反应可得到厨房内常用的一种调味品和物质E;C在农业上可用来配制波尔多液,且C和D反应可制得B;A和D反应与A和小苏打反应得到的产物完全相同.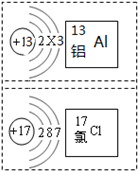 如图是铝和氯两种元素的有关信息,根据图示回答有关问题:
如图是铝和氯两种元素的有关信息,根据图示回答有关问题: