题目内容
8.化肥硝酸铵的化学式为(NH4NO3).试求:(1)硝酸铵中N、H、O三种元素的质量比7:1:12;
(2)为了保证某一农作物获得3.5kg氮元素,则需要10kg硝酸铵.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)利用元素的质量等于物质的质量与该元素的质量分数的乘积进行分析解答.
解答 解:(1)硝酸铵中N、H、O三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:7:1:12;
(2)NH4NO3中氮元素的质量分数=$\frac{14×2}{14×2+1×4+16×3}×100%$=35%
设需要硝酸铵的质量是x.则x×35%=3.5kg.
x=10kg
故填:10.
点评 本题考查学生根据化合物中各元素质量比和物质中某元素的质量分数进行分析解题的能力.

练习册系列答案
相关题目
19.下列实验方法无法达到实验目的是( )
| A. | 用肥皂水鉴别硬水和软水 | |
| B. | 用燃着的木条鉴别氮气与二氧化碳 | |
| C. | 用向上排空气法收集氧气和二氧化碳 | |
| D. | 用紫色石蕊试液鉴别稀硫酸和蒸馏水 |
16.下列实验操作正确的是( )
| A. | 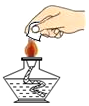 | B. | 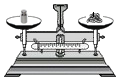 | C. | 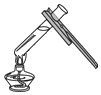 液体加热 | D. | 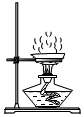 |
3.不会对人类的生存环境造成危害的是( )
| A. | 汽车排放的废气 | B. | 生活污水的任意排放 | ||
| C. | 随意丢弃废旧电池 | D. | 氢气在空气中燃烧的生成物 |

 某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验,请回答问题:
某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验,请回答问题:
